1、计算题 Fe与Fe2O3的混合物2.72g,加入到50mL 1.6mol/L盐酸中恰好完全溶解,经KSCN检验,溶液不显红色,若忽略溶液体积变化,写出反应的离子方程式??, ??,??。
反应后溶液中Fe2+物质的量浓度是??mol/ L
参考答案:(离子方程式各1分) Fe + 2H+ ="==" Fe2+ + H2? Fe2 O3 +6H+?="=" 2Fe2+ +3 H2O? Fe +2Fe3+="=3" Fe2+
0.8 mol/ L(4分)
本题解析:略
本题难度:一般
2、计算题 试简述在FeSO4溶液中加入NaOH溶液的现象,并写出有关反应的化学方程式。
参考答案:产生白色絮状沉淀,然后迅速变成灰绿色,最终变为红褐色沉淀:
FeSO4+2NaOH===Fe(OH)2↓+Na2SO4? 4Fe(OH)2+O2+2H2O===4Fe(OH)3
本题解析:本题能力层次为B。Fe(OH)2容易被氧化成 Fe(OH)3,要记住特征的颜色变化。答案是:产生白色絮状沉淀,然后迅速变成灰绿色,最终变为红褐色沉淀:
FeSO4+2NaOH===Fe(OH)2↓+Na2SO4? 4Fe(OH)2+O2+2H2O===4Fe(OH)3
学法指导:为了更好地看清楚Fe(OH)2颜色状态,做实验时:①FeSO4溶液、NaOH溶液是新配制,且用冷开水配制,可减少O2溶入量。②FeSO4溶液中加铁钉防止Fe2+氧化成Fe3+。③用长的胶头滴管吸取NaOH溶液,然后插入FeSO4溶液液面下缓慢挤压滴出。
本题难度:简单
3、填空题 某混合物A含KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列转化
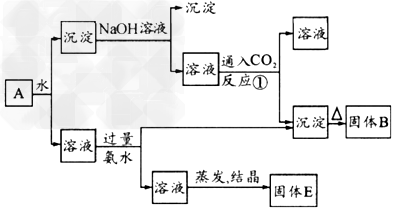
?已知:AlO2-只存在于强碱性的溶液中,遇酸性物质可生成Al(OH)3沉淀。 ?
据此回答: ?
(1)固体B所含物质的化学式____。 ?
(2)固体E所含物质的化学式____。 ?
(3)反应①的离子方程式____。
参考答案:(1)Al2O3
(2)(NH4)2SO4、K2SO4
(3)AlO2-?+2H2O?+CO2=Al(OH)3↓+HCO3-
本题解析:
本题难度:一般
4、选择题 在酸性溶液中,下列各组离子能大量共存的是(? )
A.Fe3+、NO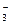 、Cl-、Al3+
、Cl-、Al3+
B.Fe3+、Cl-、I-、K+
C.Fe2+、K+、SO 、NO
、NO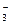
D.Fe2+、SO 、K+、MnO
、K+、MnO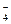
参考答案:A
本题解析:A选项符合题意;B选项中Fe3+和I-能发生氧化还原反应;C、D选项中Fe2+在酸性条件下能被NO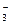 、MnO
、MnO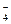 氧化。
氧化。
本题难度:简单
5、选择题 在一定条件下,下列物质的转变不能一步完成的是( )
A.Na2CO3→CaCO3
B.Fe2O3→Fe
C.CaO→Ca(OH)2
D.CuO→Cu(OH)2
参考答案:D
本题解析:
本题难度:简单