1、选择题 下列关于难溶电解质溶液说法正确的是 (? )
A.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
B.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol・L-1盐酸、③0.1 mol・L-1氯化镁溶液、④0.1 mol・L-1硝酸银溶液中,Ag+浓度:①>④=②>③
C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl-
D.25 ℃时,在Mg(OH)2悬浊液中加入少量的NH4Cl固体后,c(Mg2+)增大
参考答案:C D
本题解析:A、在含有BaSO4沉淀的溶液中存在沉淀溶解平衡,溶度积一定温度下是常数,加入Na2SO4固体后硫酸根离子浓度增大,平衡逆向进行,钡离子浓度减小,故A错误;
B、相同温度下,氯化银在水溶液中存在沉淀溶解平衡,依据溶度积是常数,与①蒸馏水相比较,②中0.1 mol・L-1盐酸溶液中氯离子0.1mol・L-1,抑制沉淀溶解平衡,银离子浓度减小;③中0.1 mol・L-1氯化镁溶液中氯离子浓度为0.2mol・L-1,平衡逆向进行,银离子浓度减小;④中0.1 mol?L-1硝酸银溶液中,银离子浓度为0.1mol・L-1,平衡逆向进行,银离子浓度增大,则Ag+浓度:④>①>②>③,故B错误;
C、硫化银溶解度小于氯化银,可以实现沉淀转化,则向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-=Ag2S↓+2Cl-,故C正确;
D、氢氧化镁溶液中存在沉淀溶解平衡,氯化铵水解显酸性,与氢氧根离子结合,促进平衡向溶解方向进行,所以镁离子浓度增大,故D正确;
故选CD.
本题难度:一般
2、选择题 将适量AgBr固体溶在水中,溶液中存在AgBr(s)  Ag+(aq)+Br-(aq)。则下列说法正确的是( )
Ag+(aq)+Br-(aq)。则下列说法正确的是( )
A.向此体系中滴加足量浓NaCl溶液,发现沉淀转化为白色,说明Ksp(AgCl)<Ksp(AgBr)
B.向此体系中加入少量AgBr固体,平衡正向移动,当再次平衡时c(Ag+)、c(Br-)增大
C.此体系中一定存在c(Ag+)=c(Br-)=[Ksp(AgBr)]1/2
D.某溶液中c(Ag+)・c(Br-)=Ksp(AgBr),说明此时c(Ag+)=c(Br-)
参考答案:C
本题解析:A项,转化成白色沉淀,不能说明Ksp(AgCl)<Ksp(AgBr),错误;B项,平衡不移动,且c(Ag+)、c(Br-)不变化;C项,根据Ksp(AgBr)=c(Ag+)・c(Br-)判断,正确;D项,当c(Ag+)・c(Br-)=Ksp(AgBr),说明此时正好形成AgBr的饱和溶液,错误。
本题难度:一般
3、计算题 化学能与电能之间的相互转化与人的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2  Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
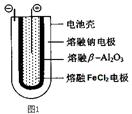
充电时,__________(写物质名称)电极接电源的负极;
该电池的电解质为________ _。
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
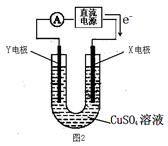
①Y电极材料是 ,发生 (填“氧化或还原”)反应。
②电解过程中X电极上发生的电极反方应式是:
③如在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是
(3)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为______________。
参考答案:(14分)
(1)Fe2++2e-= Fe(2分),钠(1分),β―Al2O3(1分)
(2)①石墨(1分),氧化(1分)
②Cu2++2e-=Cu(2分)、2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-(2分)
③0.448L或448mL(2分)没有单位扣1分
(3)2.16x10-7. (2分)
本题解析: (1)对氧化还原反应,含化合价降低的元素发生还原反应做正极。充电时负极连接阴极。能导电的做电解质溶液。
(2)由加入0.98g氢氧化铜粉完全溶解,所得溶液与电解前完全相同。可知溶液电解氢氧化铜,在阴极放电的是Cu2+,在阳极放电的是OH-。小苏打(NaHCO3)
Cu SO4 + 2 H2O= Cu(OH)2+H2SO4 n=0.98g/98gmol-1=0.01mol
2NaHCO3+H2SO4=Na2SO4+H2O+2CO2↑
0.01mol 0.02mol
0.02mol×22.4L/mol=0.448L
(3) 等体积的BaCl2溶液与2.0×10-3mol/l的Na2SO4溶液混合
Ksp=c(Ba2+)c(SO42-)=c(Ba2+)1.0×10-3=1.08×10-10
c(Ba2+)=1.08×10-7 c原(Ba2+)=2.16x10-7.
考点:本题考查电解池知识和Ksp的计算等知识。
本题难度:困难
4、填空题 某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀,从而将其除去的可能性,查得如下资料:(以下数据和实验均指在25℃下测定)
难溶电解质
| CaCO3
| CaSO4
|
Ksp(mol2・L-2)
| 3×10-9
| 9×10-6
|
?
实验步骤如下:
①往100 mL 0.1 mol・L-1的CaCl2溶液中加入100 mL 0.1 mol・L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液.
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液.
④向沉淀中加入足量的盐酸。
(1)步骤①所得悬浊液中[Ca2+]=________ mol・L-1
(2)写出第②步发生反应的离子方程式:________________________________.
(3)设计第③步的目的是________________________________________________.
(4)第④步操作发生的现象为:?。
参考答案:(1)0.003
(2)CO32- (aq)+CaSO4(s)= SO42- (aq)+CaCO3(s)
(3)洗去沉淀中附着的SO42-
(4)沉淀完全溶解,有气泡冒出
本题解析:步骤①产生白色沉淀,确定为CaSO4,根据其Ksp解得[Ca2+] =0.003 mol/L;结合两者的溶度积确定当加入固体Na2CO3时,产生CaCO3,确定②的离子方程式为CO32- (aq)+CaSO4(s)=SO42- (aq)+CaCO3(s) 。
本题难度:一般
5、选择题 下列对沉淀溶解平衡的描述正确的是( )
A.反应开始时,溶液中各离子浓度相等
B.沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等
C.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变
D.沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解
参考答案:A、反应开始时,各离子的浓度没有必然的关系,故A错误;
B、沉淀的速率和溶解的速率相等,沉淀溶解达到平衡,故B正确;
C、沉淀溶解达到平衡时,溶液中溶质的离子浓度保持不变,但不一定相等,与难溶二者是否是1:1型有关、与溶解难溶物质的溶液中是否存在难溶物质的离子等有关,故C错误;
D、沉淀溶解达到平衡时,如果再加入难溶的该沉淀物,由于固体的浓度为常数,故平衡不发生移动,故D错误;
故选B.
本题解析:
本题难度:一般