1、填空题 已知:2SO3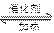 2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题:
2SO2+O2,在起始时体积相同的容器A和B中,同时分别充入2molSO3(两容器装有催化剂)。在反应过程中,A保持温度和容积不变;B保持温度和压强不变。回答下列问题:
(1)反应达平衡所需时间A?B(大于;等于;小于);达平衡时SO3的转化率
A?B(大于;等于;小于)。
(2)若平衡后,向A、B中分别充入惰性气体,?容器的平衡将向?方向移动;若平衡后,向A、B中分别充入等物质的量SO3,重新达平衡时,两容器中的SO3转化率变化情况是(填变大、变小、不变)A?,B?
参考答案:
(1)小于;小于(各1分,共2分)
(2)B;正反应;变小;不变(各1分,共4分)
本题解析:
本题考查化学平衡移动;2SO3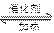 2SO2+O2,是一气体总物质的量增大的反应。(1)相同温度下,充入SO3,A容器保持体积不变,压强变大;B容器保持压强不变,体积增大,达到平衡状态时转化为状态C(如下图),故达到平衡所用时间,A小于B;假设B中的活塞不移动,由于A、B两个容器的体积、温度相同,达到平衡时A、B两容器中存在的平衡是等效平衡,其中SO3的转化率也相等。对于B和C两个状态,B中压强小于C中压强,因此C中SO3转化率大于B中SO3转化率。由此可以判断出C中SO3的转化率也大于A中SO3的转化率, 故达到平衡时,SO3的转化率 A小于B。
2SO2+O2,是一气体总物质的量增大的反应。(1)相同温度下,充入SO3,A容器保持体积不变,压强变大;B容器保持压强不变,体积增大,达到平衡状态时转化为状态C(如下图),故达到平衡所用时间,A小于B;假设B中的活塞不移动,由于A、B两个容器的体积、温度相同,达到平衡时A、B两容器中存在的平衡是等效平衡,其中SO3的转化率也相等。对于B和C两个状态,B中压强小于C中压强,因此C中SO3转化率大于B中SO3转化率。由此可以判断出C中SO3的转化率也大于A中SO3的转化率, 故达到平衡时,SO3的转化率 A小于B。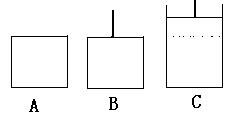
(2)达到平衡后,分别充入惰性气体,A容器体积不变,反应体系的浓度不变,平衡不移动,B容器保持压强不变,体积增大,平衡向右移动;如果充入SO3,A容器保持体积不变,压强变大,SO3的转化率减小,B中充入SO3,与原平衡为等效平衡,SO3的转化率不变。
本题难度:一般
2、选择题 可逆反应:2A(气) + 3B(气)  3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是:?
3C(气),一定条件下,在一密闭、恒容的容器中,使一定量A和B气体反应,下列叙述能用来判断达到平衡状态的是:?
A.各物质的浓度之比为c(A):c(B):c(C) = 2:3:3?
B.气体的总体积是反应开始时的 3/5?
C.混合气体的密度不变
D.单位时间内, 若消耗了 a mol A 物质, 同时也消耗了 1.5 a mol 的C物质
参考答案:D
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,A、B不能说明。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,⑤不正确,因此C不能说明;D中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,可以说明,答案选D。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:简单
3、填空题 (1)把a、b、c、d 四块金属片浸入稀H2SO4中,分别用导线两两相连可以组成原电池。a、b相连时,导线上电子由 a→b;c、d相连时,电流由 d→c; a、 c相连时 c极上产生大量气泡; b、 d相连时,d极发生氧化反应。这4种金属的活动性由强到弱的顺序是_______________
(2)王同学想在钥匙上镀上一层铜,设计电解实验时,钥匙应和电源的?极相连。
(3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式:?
碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:?
(4)用惰性电极电解饱和食盐水,当电源供给0.2mol电子时,停止通电。若此时溶液体积为2L,则所得电解液的pH是?。(不考虑气体的溶解)
(5)将含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,则另一个极上放出气体(标准状况下)为?L。
参考答案:(1)(2分)a>c>d>b?(2)(1分)负?
(3)(每空2分)Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑?
Mg(OH)2↓+H2↑+Cl2↑?
Cu+H2O Cu(OH)2+H2↑
Cu(OH)2+H2↑
(4)(2分)13
(5)(2分)5.6L
本题解析:(1)a、b相连时,导线上电子由 a→b,说明a比b活泼;c、d相连时,电流由 d→c,说明c比d活泼; a、 c相连时 c极上产生大量气泡,说明a比c活泼; b、d相连时,d极发生氧化反应,说明d比b活泼,故这4种金属的活动性由强到弱的顺序是a>c>d>b;(2)王同学想在钥匙上镀上一层铜,根据电解池的原理,钥匙应该作为电解池的阴极,阴极接电源的负极;3)碳作阳极,铜作阴极电解MgCl2溶液的离子方程式为:Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑,碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:Cu+H2O
Mg(OH)2↓+H2↑+Cl2↑,碳作阴极,铜作阳极电解硫酸钠溶液的化学方程式:Cu+H2O Cu(OH)2+H2↑;(4)用惰性电极电解饱和食盐水的反应式为:2NaCl+2H2O=Cl2↑+H2↑+2NaOH,该反应转移的电子数为2,所以当电源供给0.2mol电子时,生成的0.2molNaOH,即c(OH-)=0.2/2=0.1mol/L,c(H+)=10―13mol・L-1,所以pH=-lgc(H+)=13;(5)含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,电解该溶液时,在阴极上析出铜离子,在阳极是首先是氯离子放电,生产了氯气,接下来是氢氧根放电生产氧气,其电极方程式为:2Cl--2e-=Cl2↑,4OH--4e-=2H2O+O2↑,一个极析出0.3mol红色物质,即转移的电子数为0.6mol,所以生成了0.4/2=0.2mol的氯气和(0.6-0.4)/4=0.05mol的氧气,所以另一个极上放出气体(标准状况下)为(0.2+0.05)×22.4=5.6L。
Cu(OH)2+H2↑;(4)用惰性电极电解饱和食盐水的反应式为:2NaCl+2H2O=Cl2↑+H2↑+2NaOH,该反应转移的电子数为2,所以当电源供给0.2mol电子时,生成的0.2molNaOH,即c(OH-)=0.2/2=0.1mol/L,c(H+)=10―13mol・L-1,所以pH=-lgc(H+)=13;(5)含有0.4mol Cu(NO3)2和0.4mol KCl的溶液1 L,用铂电极电解一段时间后,在一个极析出0.3mol红色物质,电解该溶液时,在阴极上析出铜离子,在阳极是首先是氯离子放电,生产了氯气,接下来是氢氧根放电生产氧气,其电极方程式为:2Cl--2e-=Cl2↑,4OH--4e-=2H2O+O2↑,一个极析出0.3mol红色物质,即转移的电子数为0.6mol,所以生成了0.4/2=0.2mol的氯气和(0.6-0.4)/4=0.05mol的氧气,所以另一个极上放出气体(标准状况下)为(0.2+0.05)×22.4=5.6L。
点评:本题考查了原电池、电解池、pH的计算,这些知识点为高考考查的重点,本题有一定的综合性,该题难度适中。
本题难度:一般
4、选择题 可逆反应X2(气) + Y2(气) ="=" 2XY(气) ,达到平衡的标志是(?)
A.当温度和压强一定时,反应混合气平均分子量不再改变;
B.当温度一定时,单位时间内生成2n mol XY,同时生成n mol Y2;
C.当温度一定时,容器总压强不随时间改变;
D.当温度一定时,任何时间内X2和Y2的物质的量之比为定值
参考答案:B
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。反应前后气体的体积不变,因此气体的总物质的量和压强始终是不变的,C不能说明;混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量和物质的量都是不变的,所以选项A不能说明;B中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确。选项D是不一定的,答案选B。
点评:该题是中等难度的试题,该题也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,如何结合具体的可逆反应灵活运用即可。
本题难度:简单
5、选择题 对于可逆反应 A(气)+2B(气)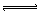 2C(气)+Q的平衡体系,下列说法错误的是?
2C(气)+Q的平衡体系,下列说法错误的是?
A.增大压强,正、逆反应的速率(v正和v逆)都增大,v正增大的倍数大于v逆增大的倍数
B.降低温度,v正、v逆都减小,v正减小的倍数大于v逆减小的倍数
C.使用催化剂,v正、v逆都改变,变化的倍数相同
D.扩大容器体积,容器内A、B、C物质的量都不变
参考答案:B、D
本题解析:本题主要讨论的是对化学反应速率影响的四个因素,即温度、压强、浓度和催化剂。在备选答案中对这四个因素均有所讨论。
①温度“升高温度”,正、逆反应速率都会增大,只不过对于是吸热反应还是放热反应增大的程度不</PGN0078B.TXT/PGN>同,具体到本题正反应为放热反应v正增大的倍数小于v逆增大的倍数,D项说法正确,但不是本题要求答案。B的说法,速率都减小是对的,但v正减小的倍数应小于v逆的倍数,所以B项说法错误,是本题要求的答案。
②压强:对于有气体参加的反应,改变压强,实质是改变浓度,反应物和产物的浓度都增加了,从反应式的各物质系数看,增大的倍数不同,反应物浓度增大的多,所以v正的速率增大的倍数大于v逆增大的倍数,A项正确,不是答案。
③扩大容器的体积等于减小压强,从而减小了体系内物质的浓度,正、逆反应速率必定改变不同,所以,A、B、C物质的量不变是不正确的,D为答案。
④催化剂使正、逆反应速率改变倍数相同,可使达到平衡的时间缩短,所以C项正确。不是本题答案。
本题难度:一般