|
高考化学知识点归纳《物质的量》考点预测(2017年强化版)(八)
2017-11-11 02:34:21
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 配制100mL、1.0mol・L-1的NaOH溶液,下列情况会导致溶液浓度偏高的是
A.读数时,俯视确定凹液面与刻度线相切
B.容量瓶使用前经蒸馏水清洗后还残留有少量蒸馏水
C.定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水
D.配制过程中,用蒸馏水洗涤烧杯和玻璃棒后,未把洗涤液移入容量瓶
|
参考答案:A
本题解析:俯视确定凹液面与刻度线相切,溶液的体积偏小,配制溶液浓度偏高,故A正确;配制最后需加水定容,故容量瓶使用前有少量蒸馏水,对所配溶液浓度无影响,故B错误;定容摇匀后,液面低于刻度线,是因为有部分溶液留在了刻度线以上,浓度不变,但继续加入水后,浓度偏低,C错误;未把洗涤液转移到容量瓶中,溶质的物质的量偏小,浓度偏低,D错误,答案选A.
考点:一定物质的物质的量的溶液配制
本题难度:一般
2、填空题 (1)将质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为______,该混合气体的平均摩尔质量为______.
(2)同温同压下,质量相同的五种气体:①CO2②H2③O2④CH4⑤SO2所占的体积由大到小的顺序是(填序号,下同)______;
所含原子数由多到少的顺序是______;密度由大到小的顺序是______.
(3)VmLAl2(SO4)3溶液中含Al3+ag,取V/4mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是(单位为mol/L)______;
(4)标准状况下将224LHCl气体完全溶于1L水中,所得溶液的密度为1.1g/cm3,则所得稀盐酸的质量分数为______,物质的量浓度为______.
参考答案:(1)根据n=计算物质的量,混合气体中N2和NO的物质的量之比为1530=1:1,
设混合气体都为1mol,则混合气体中氮原子的物质的量为3mol,氧原子的物质的量为1mol,根据N=n×NA,氮原子和氧原子的个数比为3:1,
该混合气体的平均摩尔质量为:M平均=m总n总=1mol×28g/mol+1mol×30g/mol2mol=29g/mol.
故答案为:1:1;3:1;29g/mol;
(2)根据同温同压下,物质的量与体积呈正比,气体的物质的量越多,气体的体积就越大,同温同压下,五种气体的质量相同,根据n=mM计算物质的量,
由计算公式可以看出,质量相同时,物质的量与气体的摩尔质量呈反比,即摩尔质量越大,物质的量越小,
又知:①CO2②H2③O2④CH4⑤SO2的摩尔质量由大到小的顺序为:⑤SO2、①CO2、③O2、④CH4、②H2,
所以所占的体积由大到小的顺序是②④③①⑤;
设气体的质量都是1g,则①CO2含有的原子的个数为344NA,②H2含有的原子的个数为12NA,③O2含有的原子的个数为132NA,④CH4含有的原子的个数为116NA,⑤SO2含有的原子的个数为164NA,
所以所含原子数由多到少的顺序是②④①③⑤;
根据可知:密度与摩尔质量呈正比,所以,密度由大到小的顺序是⑤①③④②,
故答案为:②④③①⑤;②④①③⑤;⑤①③④②;
(3)VmLAl2(SO4)3溶液中含Al3+ag,则n(Al3+)=,n(SO42-)=a27×32mol,
取V/4mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是:a18mol×14V×10-3L=a72V×103mol/L,故答案为:125a9V;
故答案为:125a9V;
(4)标准状况下将224LHCl的物质的量为:n(HCl)=224L22.4L/mol=10mol,则m(HCl)=10mol×36.5g/mol=365g,
溶液的质量为:365g+1000g=1365g,
所以溶液的质量分数为:365g1365g×100%=26.74%,
溶液的体积为:1365g1.1g/ml=1240.9ml,即1.2409L,
所以,溶液的物质的量浓度为10mol1.2409L=8.06mol/L,
故答案为:26.74%,8.06mol/L
本题解析:
本题难度:简单
3、填空题 同温同压下,质量相同的五种气体:①CO2?②H2?③O2?④CH4?⑤SO2
所占的体积由大到小的顺序是(填序号,下同)______;
所含原子数由多到少的顺序是______;
密度由大到小的顺序是______.
参考答案:设质量均为mg,
则物质的量分别为m44mol、m2mol、m32mol、m16mol、m64mol,
同温同压下体积与物质的量成正比,则所占的体积由大到小的顺序是②④③①⑤;
含原子的物质的量分别为3m44mol、mmol、m16mol、m4mol、3m64mol,
所含原子数由多到少的顺序为②④①③⑤;
由pM=ρRT可知,密度与摩尔质量成正比,即摩尔质量越大,密度越大,
64>44>32>16>2,即密度由大到小的顺序为⑤①③④②,
故答案为:②④③①⑤;②④①③⑤;⑤①③④②.
本题解析:
本题难度:一般
4、选择题 下列溶液中,阴离子浓度最大的是
[? ]
A.50mL?0.5mol・L-1 H2SO4溶液?
B.35mL?0.6mol・L-1? Al2(SO4)3溶液
C.70mL?0.8?mol・L-1 NaCl溶液?
D.60mL?0.7?mol・L-1?Na2CO3溶液
参考答案:B
本题解析:
本题难度:简单
5、选择题 氧气的摩尔质量为32.0 g・mol-1,由此求出的标准状况下氧气的密度可能是(? )
A.1.5 g・L-1
B.1.43 g・L-1
C.1.293 g・L-1
D.1.2 mg・L-1
参考答案:B
本题解析:根据密度公式ρ=M/Vm得:
ρ(O2)=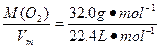 ="1.43" g・L-1 ="1.43" g・L-1
本题难度:简单
|