1��ѡ���� ����˵������ȷ���ǣ� ? ��
A������������ŷŻ��������ЧӦ
B����ɫʳƷ�Dz����κλ�ѧ���ʵ�ʳƷ
C��Cu��ŨH2SO4��Ӧ��H2SO4�����������ԣ��ֱ�������
D���ü��ȵķ������ܼ���NaHCO3��Na2CO3����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� 2010��4��14�ճ����緢�ı�����ɽ�����Ļ�ɽ�ң���Ҫ���ж���������������������ʣ������纽��ҵ�����˾�ľ�����ʧ�������й����仯�����˵������ȷ����
[? ]
A����ɽ�緢�����Ļ�ɽ���в����ܺ���SO3����
B�������ʵ�����SO2��Cl2ͬʱͨ��ˮ�У�������Һ��Ư������ǿ��pH��С
C����ͬ������SO2��SO3�з�����֮��Ϊ1:1
D��һ�������£������۷���SO3��ˮ��Ӧ����Һ�У����Եõ���������
�ο��𰸣�D
���������
�����Ѷȣ���
3������� ���һ����ܾ֡�����������ָ��������SO2���ŷź������ˮ�Ĵ�����
�ҹ���ʮһ�塱�ڼ价����������Ҫ������ش��������⣺
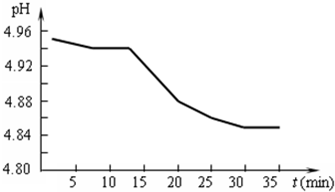
��1��SO2���ŷ�������������Ҫ���أ�ij��������pH��ʱ��ı仯����ͼ��ʾ�����û�ѧ����ʽ��ʾ�õ�������pH��ʱ�����Ӷ���С��ԭ��______��
��2�����Ͱ����������������ð�����������SO2����������狀���������泥�����һ������������з�Ӧ����SO2���ü����ϴ�ͳ��NaOH��Һ���ռ���H2SO4����SO2�����������ŵ���______��
��3��Ϊ��һ������SO2����Ⱦ�����Ϊ������������̽����CO��ԭSO2�õ�������ķ�������ȥSO2���÷����漰���Ļ�ѧ��ӦΪ��SO2+2CO=2CO2+
Sx��CO+Sx=COS��2COS+SO2=2CO2+Sx������COS���ʻ����ӵĵ���ʽΪ______��
��4��������ˮ�к�����ϸС��������ɼ���ijЩ����ʹ֮�ۼ��ɽϴ�Ŀ����������������һ�ֳ�������ʹ������ˮ��������۳������ʣ��仯ѧʽΪ______����������ˮ�к������ĵ������ͨ��������Ĥ�ѵ����ս��д���������������ϸ���������½�NH4+����ΪNO3-��NH4++2O2=NO3-+2H++H2O��Ȼ���ڸ�������Һ�м���״���NO3-�ͼ״�ת��Ϊ���������壮��д������״���Ӧ�����ӷ���ʽ______��
�ο��𰸣���1��ij��������pH��ʱ��ı仯��������ʱ����������ҺPH��С��֤��������Ũ�����������γ��Ƕ�����������ˮ���������ᣬ�����ᱵ��������Ϊ���ᣬ������仯Ϊǿ�ᣬ��Һ��������Ũ������PH��С����Ӧ�Ļ�ѧ����ʽΪ��2H2SO3+O2=2H2SO4���ʴ�Ϊ��2H2SO3+O2=2H2SO4��
��2�����ð�����������SO2����������狀���������泥�����Ϊ���ϣ�������Ⱦ���ﵽ���������Դ��Ŀ�ģ����Ϊ�ʣ����������Դ��������Ⱦ��
�ʴ�Ϊ�����ܻ�������SO2�����ܵõ����Ϸ���泥�
��3��C�ķǽ�����С��O��S���ṹʽΪO=C=S��C�Ļ��ϼ�Ϊ+4�ۣ����ԭ�ӽṹд������ʽΪ��

��
�ʴ�Ϊ��

��
��4���������������������γɵĽ�����нϴ������������������ʵ����ã���������ʹ������ˮ��������۳����������������̷��������εȣ�����ϸ���������½�NH4+����ΪNO3-��NH4++2O2=NO3-+2H++H2O��Ȼ���ڸ�������Һ��������Һ������ǿ�����ԣ�����״�����������Ӻ��������������״�Ϊ������Ϊ������̼��NO3-�ͼ״�ת��Ϊ���������壬�ƶ����ᱵ��ԭΪ��������Ӧ�����ӷ���ʽΪ��6NO3-+5CH3OH+6H+=3N2��+5CO2��+13H2O��
�ʴ�Ϊ��KAl��SO4��2?12H2O��?FeSO4?7H2O��? 6NO3-+5CH3OH+6H+=3N2��+5CO2��+13H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ������ָpHΪ���ٵ���ˮ��������
A��pH��5.6
B��pH��5.6
C��7��pH��5.6
D��pH=7
�ο��𰸣�A
���������
�����Ѷȣ���
5������� �γ������ԭ��֮һ�ɱ�ʾ���£�

�Իش��������⣺
��1��ͼ��������Ӧ������������ԭ��Ӧ����______�����ţ���
��2���ӱ��������ĽǶȳ�������ҵ����Ŭ������������ĸ�Դ���������������Լ�С�������Ⱦ������һ�ǽ�SO2��+4����Ԫ�ر��0����Ԫ�أ�������һԭ�������ڹ������̵�����ͨ����ʵ�______�������������ԭ��������ȥSO2����������һЩ�����ù����İ�ˮ��NH3?H2O������SO2���˻�ѧ��Ӧ�IJ�����______��
��3���������糧ȼ��ú�ķ�������������SO2��O2��N2��CO�ȣ�Ϊ�˳�ȥ�к�����SO2�����Ϊ���������÷�ĩ״��̼��ƻ���ʯ�ҵ�����Һϴ�ӷ�������Ӧ����Ϊ����Ƶȣ�д����CaCO3����Һϴ�����������Ļ�ѧ����ʽ��______��
�ο��𰸣���1����������ȼ�����ɶ���������������ԭ��Ӧ��������������Ϊ����������������ԭ��Ӧ��������������ˮ���������ǻ��Ϸ�Ӧ����Ӧ��������Ԫ�ػ��ϼ۱仯���Ƿ�������ԭ��Ӧ��
�ʴ�Ϊ���ۣ�
��2����С�������Ⱦ������һ�ǽ�SO2��+4����Ԫ�ر��0����Ԫ�أ�������һԭ�������ö�������������ԣ�����ͨ�뻹ԭ����ԭ���������ȥ���������ù����İ�ˮ��NH3?H2O������SO2����������������������ͼӦ�����κ�ˮ����ˮ������Ӧ����������狀�ˮ��
�ʴ�Ϊ����ԭ����������李�ˮ��
��3����������������SO2��O2��N2��CO�ȣ�Ϊ�˳�ȥ�к�����SO2�����Ϊ���������÷�ĩ״��̼��ƻ���ʯ�ҵ�����Һϴ�ӷ�������Ӧ����Ϊ����Ƶȣ���������������������������������̼��Ʒ�Ӧ��������ƺͶ�����̼д���������ķ�ӦΪ��2SO2+O2+2CaCO3�T2CaSO4+2CO2��
�ʴ�Ϊ��2SO2+O2+2CaCO3�T2CaSO4+2CO2��
���������
�����Ѷȣ�һ��