| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ���⡶��������Ƶ����Ԥ�⣨2017�����°棩(��)
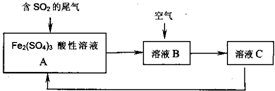 �ο��𰸣�D ��������� �����Ѷȣ�һ�� 2������� ������ʶ��Ӧ�����ʳ������������֣�һ�Ǵ����ʵ������ʶ�����ʿ��ܸ���Щ���ʷ�����Ӧ�����Ǵ���������Ԫ�صĻ��ϼ۷����������Ƿ���������Ի�ԭ�ԣ���ͼ����Ԫ�صĸ�����̬���������Ķ�Ӧ��ϵ�� �ο��𰸣���1��A�е�S�Ļ��ϼ�Ϊ+6���ҿ���ת��Ϊ���ᣬ�ֿ��ԺͶ���������ת�������AΪ��������B�е���Ļ��ϼ�Ϊ-2�ۣ���Ϊ��̬�⻯����BΪ���⣬ ��������� �����Ѷȣ�һ�� 3��ѡ���� ������������γ�������ǣ������� �ο��𰸣�C ��������� �����Ѷȣ��� 4��ѡ���� ��ͼ��ijú���糧����������װ��ʾ��ͼ������˵��������ǣ������� |
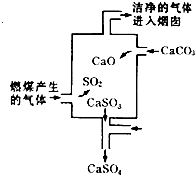
�ο��𰸣�B
���������
�����Ѷȣ���
5������� �±��Dz��ֳ���ij�տ��������ձ���
| ���� | ��Ⱦָ�� | ��Ҫ��Ⱦ�� | ���������ȼ� SO2 NO2 PM10 A 98 23 67 SO2 �� B 47 29 35 SO2 �� C 62 40 113 PM10 �� D 42 76 59 NO2 �� | ||
�ο��𰸣���1������ͼ��Ԥ�����ʺ����ݿ�֪�漰����Ⱦ����Ҫ�Ƕ�������������������������������Ⱦ�ﺬ����֪����������A��ߣ����γ����ꣻ
�ʴ�Ϊ������������������A��
��2����������֮һ���������������ϼ�װ����ת��������ʹCO��NOx��Ӧ���ɿɲ��������̬����ѭ����������Ϊ�����Ͷ�����̼���壻
�ʴ�Ϊ�������Ͷ�����̼��
��3������������������������Һ���պ���������Ĺ�ҵ�������÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ��SO2+2NaOH=Na2SO3+H2O��
�ʴ�Ϊ��SO2+2NaOH=Na2SO3+H2O��
�ڶ�������ͨ��һˮ�ϰ���Һ�з�Ӧ����������李���������李�����李�������泥�����������隣�����Ϊ����泥���������隣�����Ϊ������泥���Ӧ�Ļ�ѧ����ʽΪ��2��NH4��2SO3+O2=2��NH4��2SO4��
�ʴ�Ϊ��2��NH4��2SO3+O2=2��NH4��2SO4��
���������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���������л���ѧ��.. | |
| �����Ŀ |