1������� �������⣩��ҵ�ϸ�����ˮ���������ʻ����ӵIJ�ͬ���ж��ִ������������磺
| ��ˮ���������� | ��������
H+��OH-
�кͷ�
Cu2+��Hg2+
������
CN-
������ԭ��
|
��ش�
��1�����кͷ��У�����CO2��������ˮ�������ӷ���ʽ��______��
��2���ڳ������У���������������������Ч�ش�����Cu2+��Hg2+���ؽ������ӵ���ˮ����ij��ˮ���������Ʒ�Ӧ��������ֻ��Hg2+���Һ���Ϊ400mg/L������10L��������ˮ������Ҫ��������______g����ȷ��0.1����
�ҹ��涨Hg2+���ŷű����ܳ���0.05mg/L����1L��ˮ����������������Hg2+Ϊ2��10-7mol�������ˮ�Ƿ�ﵽ���ŷű�______����ǡ�����
��3����������ԭ���У�����Cl2������ˮ�е��ж�����CN-���ɵõ�������CO2��N2�����μӷ�Ӧ��Cl2��CN-�����ʵ���֮��Ϊ5��2����÷�Ӧ�����ӷ���ʽ��______��
�ο��𰸣���1�������кͷ�������ˮ����Ӧ����Һ���������ԣ�������Ӧ���ڴ�����NaHCO3����Na2CO3��Һ�ʼ��ԣ�����ΪNa2CO3�����Է�Ӧ�����ӷ���ʽӦΪCO2+OH-�THCO3-����д��CO2+2OH-�TCO32-+H2O����������Ҫ��
�ʴ�Ϊ��CO2+OH-�THCO3-��д��CO2+2OH-�TCO32-+H2O�����֣���
��2��10L��������ˮ�к���Hg2+������Ϊ10L��400mg/L=4000mg����4g�����ʵ���Ϊn��Hg2+��=4g200g/mol=0.02mol��
��Ӧ�����ӷ���ʽΪHg2++S2-=HgS����n��Na2S��=n��S2-��=n��Hg2+��=0.02mol��
������0.02mol��78g/mol=1.56g��1.6g��
��1L��ˮ����������������Hg2+Ϊ2��10-7mol����1L��ˮ��Hg2+����Ϊ��2��10-7mol��200g/mol=4��10-5g��
��0.04mg��0.05mg�������ˮ�ﵽ���ŷű���
�ʴ�Ϊ��1.6���ǣ�
��3��������֪��Ӧ��ΪCl2��CN-��������ΪCO2��N2���Ҳμӷ�Ӧ��Cl2��CN-�����ʵ���֮��Ϊ5��2�����������غ㶨�ɿ�֪����Ӧ���л�Ӧ��H2O����Ӧ�����ӷ���ʽΪ
5Cl2+2CN-+4H2O�T10Cl-+2CO2+N2+8H+���ʴ�Ϊ��5Cl2+2CN-+4H2O�T10Cl-+2CO2+N2+8H+��
���������
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ��д����ȷ���ǣ�������
A���ô����ܽ�̼��ƣ�2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2��+H2O
B��̼�������Һ�м��������ȵ�����������Һ��NH4++OH-=NH3��+H2O
C���������Ƶ�������Һ��H2O2������ȡClO2��4ClO3-+4H2O2+4H+=4ClO2��+3O2��+6H2O
D���������ữ�Ľۺ�ɫ���ظ���أ�K2?Cr2O7����Һ���Ҵ�������������Ͳ���ɫ���۸��������ڼ���Ƿ�ƺ��ʻ��2Cr2O72-+3C2H5OH+16H+��4Cr3++3CH3COOH+11H2O
�ο��𰸣�A���ô����ܽ�̼��Ƶ����ӷ�ӦΪ2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2��+H2O����A��ȷ��
B��̼�������Һ�м��������ȵ�����������Һ�����ӷ�ӦΪHCO3-+NH4++2OH-=NH3��+2H2O+CO32-����B����
C���������Ƶ�������Һ��H2O2������ȡClO2�����ӷ�ӦΪ2ClO3-+H2O2+2H+=2ClO2��+O2��+2H2O����C����
D������Ƿ�ƺ��ʻ�����ӷ�ӦΪ2Cr2O72-+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O����D��ȷ��
��ѡBC��
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ�Ӧ�У�������ȷ����
[? ]
A����AlCl3��Һ�м��������ˮ��Al3++3NH3��H2O=Al(OH)3��+3NH4+
B���ô����ܽ�CaCO3��CaCO3+2H+=Ca2++CO2��+H2O
C����Ba(OH)2��Һ�еμ�NaHSO4��Һ�����ԣ�2H++SO42-+Ba2++2OH-=BaSO4��+2H2O
D����Mg(HCO3)2��Һ�м����������ʯ��ˮ��Mg2++2HCO3-+Ca2++2OH-=CaCO3��+MgCO3��+2H2O
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
4��ѡ���� ���л�ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����������ƯҺ�м�Ũ�������������ClO�� + Cl��+2H+=Cl2��+H2O
B������SO2ͨ��Ca(ClO)2��Һ�У�SO2+H2O+Ca2++2ClO-=CaSO3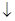 +2HClO
+2HClO
C����ϡHNO3�ܽ�FeS���壺FeS+2H+=Fe2++H2S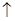
D������������Һ������ʵ�����ϡ�����ϣ�Ca2++OH-+H++SO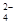 =CaSO4
=CaSO4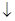 +H2O
+H2O
�ο��𰸣�A
���������A��ȷ��B����CaSO3���л�ԭ���ܱ�HCLO����������ƣ�C�����������ǿ������������FeS���壻D������ȷΪ��Ca2++2OH-+2H++SO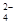 =CaSO4
=CaSO4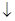 +2H2O��
+2H2O��
�����Ѷȣ�һ��
5��ѡ���� �±������ۺ������ǣ�
ѡ��
| ��ѧ��Ӧ�������� ����ʽ ����ʽ
| ��?��
|
A
| NaHSO4��Һ��Ba(OH)2��Һ��Ӧ�����ԣ�
2H++SO42��+Ba2��+2OH�� = BaSO4�� + 2H2O
| ��ȷ
|
B
| ��̼��þ��Һ�м�������ϡ���
CO32-��2H��=CO2����H2O
| ����̼��þ��Ӧд��������ʽ
|
C
| ���ˮ�еμӱ��͵��Ȼ�����Һ��Һ���Ϊ���ɫ��
Fe3��+3H2O = Fe��OH��3��+3H��
| ��ȷ
|
D
| NaOH��Һ��ͨ������CO2��Ӧ��OH-��CO2=HCO3��
| ��ȷ
|
?
�ο��𰸣�A
�����������
�����Ѷȣ�һ��