1��ѡ���� ���и����ʵĻ�ѧʽ�����ƣ����������������ȷ����
A.FeO ?������ ?�������������
B.Na2CO3 ?С�մ� ?��
C.CuSO4������ ?ͭ�ᡡ������
D.CO2 ?�ɱ� ?����������
�ο��𰸣�D
������������������A�е�FeO����������������B�е�Na2CO3�����մ�C�е�CuSO4�����Σ����������ѡD��
���㣺���ʵ���������
�����������ص㿼�������������⡣
�����Ѷȣ�����
2������� A��B��C��D��EΪԪ�����ڱ��ж�����Ԫ���γɵ��������ӣ�A��B��C��D�������ӵĵ���������E�ĵ�������8��
��1��A��B��ϳɵĻ�������м������Ӽ����й��ۼ���A��C��ϳɵĻ�������������ˮ�������ڼ�ˮ��Һ����ɫ����Һ��CԪ�������ڱ��е�λ��Ϊ ?_?�������ˮ��Һ��Ӧ�����ӷ���ʽΪ__________________________________��
��2��B��E��ϳɻ������������������֮��Ϊ2��1��A��D��ϳɻ����ﶡ���������Ӧ������ɫ��ζ�����壬����ĵ���ʽΪ��? _?��1molD����������? _?mol����
��3����һ��Һ̬���⻯�����죬�������E�ĵ�������ͬ���ǡ������ߺš��ɴ�����ʱʹ�õĸ���ȼ��֮һ���ṹ�������ָ÷��ӽṹ��ֻ�е������백���ƣ����� �ĽṹʽΪ? ___��
�ο��𰸣���1����3���ڢ�A? Al(OH)3+OH-=AlO2-+2H2O
��2��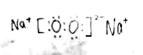 ? 11mol
? 11mol
��3��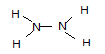
�����������1����������Ϊ10�����ӵ������ӣ�N3-��O2-��F-��OH-��NH2-�� �����ӣ�Na+��Mg2+��Al3+��NH4+��H3O+����������Ϊ18�����ӵ������ӣ�S2-��O22-��Cl-��HS-�� �����ӣ�K+��Ca2+��N2H5+��N2H62+�����������⣬A��B��C��D����10e-���ӣ�EΪ18e-���ӣ�A��B�γɵĻ�������м������Ӽ����й��ۼ���10e-�������γɵĻ�����������Ӽ����й��ۼ�������Ϊ���λ��������A��C��ϳɵĻ�������������ˮ��10e-�����н�ϳ�������ˮ�Ļ�������Mg��OH��2��Al��OH��3���ٸ��������ڼ�ˮ��Һ����ɫ����Һ��ȷ����ΪAl��OH��3����Ϊǿ��NaOH����AΪOH-��BΪNa+��CΪAl3+����C�����ڱ��е�λ�õ������ڣ���A�塣Al��OH��3��NaOH��Ӧ����ʽΪAl��OH��3+NaOH�TNaAlO2+2H2O����д���ӷ���ʽΪAl��OH��3+OH-=AlO2-+2H2O����2���������⣬A��OH-��D��H3O+����ϳɻ����ﶡ����˶�ΪH2O��B��Na+��B��E�γɵĻ������������������֮��Ϊ2��1��E����ΪS2-��O22-������Ϊ�������Ӧ������ɫ��ζ���壬���Ա�ֻ��ΪNa2O2������ʽ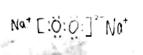 1mol H3O+��11mol���ӡ�
1mol H3O+��11mol���ӡ�
��3���������⣬��������ΪҺ̬���⻯���ͬʱҲΪ18���ӣ�Nԭ�Ӻ�����7�����ӣ�Hԭ�Ӻ�����1�����ӣ���˻���������Ӧ��2��Nԭ�Ӻ�4��Hԭ�ӣ��ʻ�ѧʽΪN2H4���ṹ�����õ��÷�����ֻ���е��������Ե�ԭ�Ӻ͵�ԭ�ӡ���ԭ�Ӻ���ԭ��֮�䶼���γ�һ�Թ��õ��Ӷԣ��ʵ���ʽΪ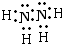 ���ṹʽ
���ṹʽ ��
��
�����Ѷȣ�һ��
3������� (ÿ��2�֣���12��)�ƶ����л�����Ļ�ѧʽ��
��X��Y��Ԫ�����γ�XY2�ͻ����XY2�й���38�����ӣ���XY2�����ӻ�����仯ѧʽ��?����XY2�ǹ��ۻ������仯ѧʽ��?��
�Ƶ��������ڣ�X��Y��Ԫ�ص�ԭ������֮��Ϊ4��������ɵ�XY�ͻ�����仯ѧʽΪ??��
��1molij���ʺ��в�ͬ��������Ԫ�ص�ԭ�Ӹ�1mol������������Ϊ20mol�������ʵĻ�ѧʽΪ??��
��ij�ǽ���X���������Ϊ+m����������������Ӧ��ˮ��������b����ԭ�ӣ���������Ļ�ѧʽ��?��
��XԪ�ص�������ۺ��۾���ֵ֮��Ϊ6��YԪ�غ�XԪ��ԭ�ӵĴ�����Ӳ��϶���8�����ӣ�X��Y�γɵĻ�������ˮ��Һ���ܵ�������Ӳ�ṹ��ͬ�����ӣ���û�������?��
�ο��𰸣�.��CaF2?CS2 ?��2��MgS?��3��NaOH �� LiHS?
��4��H2b-mXOb?��5��KCl?��CaCl2
�����������1����������ӻ��������ݻ�ѧʽ��֪X�Ļ��ϼ��ǣ�2�ۡ�Y�ǣ�1�ۡ�XY2�й���38�����ӣ������CaF2 ��XY2�ǹ��ۻ�������仯�ϼ۷ֱ��ǣ�4�ۺͣ�2�ۣ�����CS2��
��2����ɵ�XY�ͻ������Ӧ���ǵ�IA�͵ڢ�A���ڢ�A�͵ڢ�A�Լ��ڢ�A�͵ڢ�A������Ϊ���������ڣ�X��Y��Ԫ�ص�ԭ������֮��Ϊ4��������MgS��
��3�����в�ͬ��������Ԫ�أ����һ��������Ԫ�أ����Ը������������жϣ�������NaOH �� LiHS��
��4��b����ԭ�ӵĸ��۹�����2b�����Ժ��е���ԭ������2b��m������ѧʽΪH2b-mXOb��
��5��XԪ�ص�������ۺ��۾���ֵ֮��Ϊ6����X�ǵڢ�AԪ�ء�XԪ��ԭ�ӵĴ�����Ӳ�����8�����ӣ�����X����Ԫ�أ����Ի�ѧʽΪKCl ��CaCl2��
�����Ѷȣ�һ��
4��ѡ���� ��Na+������ͬ�������������������ǣ�?��
A��NH4+
B��F-
C��NH3
D��OH-
�ο��𰸣�A
��������������Ƶ�ԭ������Ϊ11����Na+����11������������ԭ�ӱ�Ϊ������Ҫʧȥ���ӣ��������Ϊ10��Ȼ���ж�ѡ�����������
A��NH4+�о���11����������10�����ӣ�����Na+������ͬ�������͵���������A��ȷ��
B��F-����9�����Ӻ�10�����ӣ�����Na+������ͬ�������͵���������B����
C��NH3����10�����Ӻ�10�����ӣ���Na+����11����������10�����ӣ���C����
D��OH-�о���9�����Ӻ�10�����ӣ�����Na+������ͬ�������͵���������D����
��ѡA��
�������⿼�����е��������͵�������ѧ��Ӧע�����������������ڵ�������������������=���������������
�����Ѷȣ�һ��
5��ѡ���� �����й���ʶ��ȷ����?��?����
A��s��p��d��f���ܼ��Ĺ����Ŀ�ֱ�Ϊ1��3��5��7
B�������Ӳ���ܼ����Ǵ�s�ܼ���ʼ�� f �ܼ�����
C�������Ӳ㺬�е��ܼ���Ϊ��n-1��
D�������Ӳ㺬�еĵ�����Ϊ2n2
�ο��𰸣�A
���������s��p��d��f���ܼ��Ĺ����Ŀ�ֱ�Ϊ1��3��5��7����A��ȷ�������Ӳ���ܼ����Ǵ�s�ܼ���ʼ�ģ�ֻ�п��IJ���д�f�ܼ�����������B�������Ӳ㺬�е��ܼ���Ϊn2����C�������Ӳ��������ɵ���������Ϊ2n2����D����ȷ�����Ա���Ĵ�ѡ��A��
���������⿼���˵��Ӳ��֪ʶ�����ڶԴ�֪ʶ�Ŀ��飬����Ƚϳ�����һ�����Ѷȡ�
�����Ѷȣ���