1��ѡ���� ��ʾ0.1mol/L NaHCO3��Һ���й���Ũ�ȴ�С�Ĺ�ϵʽ����ȷ���ǣ� ? ��
A��c��Na+����c��HCO3-����c��CO32-����c��H+����c��OH-��
B��c��Na+��+c��H+��=c��HCO3-��+2c��CO32-��+c��OH-��
C��c��Na+����c��HCO3-����c��CO32-����c��H2CO3����c��OH-��
D��c��H+����c��H2CO3����c��OH-����c��HCO3-����c��CO32-��
2��ѡ���� ����������ȷ����?
[? ]
A��c(NH4+)��ȵ�(NH4)2SO4��Һ��(NH4)2Fe(SO4)2��Һ��NH4Cl��Һ�У�����Ũ�ȴ�С��ϵ�ǣ�c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<?c(NH4Cl)
B���к���ͬ�������ͬpH�Ģ����ᡢ������͢۴���������ͬŨ�ȵ�NaOH��Һ�������ϵ��V1��V2��V3
C��0.2?mol��L-1?HCl��Һ������0.05?mol��L-1?Ba(OH)2��Һ��Ϻ���Һ��pH��1
D����֪������FeS��Ksp?=?8.1��10-17��FeS������Һ��c(H+)2��c(S2-)?=?1.0��10-22��Ϊʹ��Һ��c(Fe2+)�ﵽ��1mol/L��Ӧ������Һ�е�c(H+)Ϊ1.11��10��3mol/L
3��ѡ���� �����£���20?mL?0.2?mol/L?H2A��Һ�еμ�0.2?mol/L?NaOH��Һ���й��������ʵ����仯����ͼ������I����H2A��II����HA����III����A2����������ͼʾ�жϣ�����˵����ȷ����?
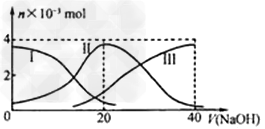
[? ]
A����V��NaOH��=20?mLʱ����Һ������Ũ�ȴ�С��ϵ��c(Na+)>c(HA����>c(H+)>?c(A2��)>c(OH��) ?
B���������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮ�Ĵ� ?
C��NaHA��Һ�У�c(OH-)��c(A2�C)��c(H+)��c(H2A)? ?
D����Na2A��Һ����ˮ�Ĺ����У�pH��������Ҳ���ܼ�С
4��ѡ���� HAΪ�����Ե��ڴ����һԪ���ᣮ��0.1?mol/L?NaA��Һ�У�����Ũ�ȹ�ϵ��ȷ����
[? ]
A��c(Na��)��c(A��)��c(H��)��c(OH��)
B��c(Na��)��c(OH��)��c(A��)��c(H��)
C��c(Na��)��c(OH��)��c(A��)��c(H��)
D��c(Na��)��c(H��)��c(A��)��c(OH��)
5��ѡ���� ijͬѧ������ʵ���Ũ�Ⱦ�Ϊ0.01mol?L?-1��CH3COOH��CH3COONa�Ļ����Һ�����Ժó����й�ϵʽ������Ϊ���в���ȷ���ǣ�������
A��c��CH3COO-����c��CH3COOH��
B��c��CH3COO-����c��Na+����c��H+����c��OH-��
C��c��Na+��=c��CH3COO-��=0.01mol?L-1
D��c��CH3COOH��+c��CH3COO-��=0.02mol?L-1