1、填空题 (18分)下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式回答以下问题:
?主族
周期
| IA
| IIA
| IIIA
| IVA
| VA
| VIA
| VIIA
| 0
|
二
| ?
| ?
| ?
| ?
| ①
| ?
| ②
| ?
|
三
| ③
| ④
| ⑤
| ⑥
| ?
| ?
| ⑦
| ⑧
|
四
| ⑨
| ?
| ?
| ?
| ?
| ?
| ⑩
| ?
|
(1)在这些元素中,最活泼的非金属元素是 ?化学性质最不活泼元素原子的原子结构示意图为? ?;
(2)元素的最高价氧化物对应的水化物中酸性最强的酸是?,
呈两性的氢氧化物是?;
(3)最强碱的电子式为:_____________?①的气态氢化物的电子式:_____________________
④和⑦所形成化合物的电子式:________________________。
(4)在⑦与⑩的单质中,化学性质较活泼的是?,可用什么化学反应说明该事实(写出反应的化学方程式):?。
来源:91考试网 www.91eXam.org
参考答案:(10分) (1)? F?(2)? HClO4? Al(OH)3
(3)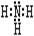 ?
?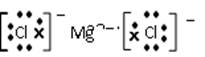
(4)Cl2? 2NaBr+Cl2=2NaCl+Br2(2分)
本题解析:(1)元素的非金属性同一周期:从左到右依次依次增强,同一主族从上倒下依次减弱,所以在这些元素中,最活泼的非金属元素是②,第二周期第七主族为F,化学性质最不活泼的是0族的稀有气体元素,表中⑧为Ar,Ar的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性根据元素周期律同一周期从左到有依次增强,
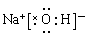 同一主族从上到下依次减弱,F无最高价氧化物,所以最强的是⑦,氯元素,最高价氧化物对应的水化物为高氯酸; HClO4?高中阶段学习的呈两性的氢氧化物为Al(OH)3
同一主族从上到下依次减弱,F无最高价氧化物,所以最强的是⑦,氯元素,最高价氧化物对应的水化物为高氯酸; HClO4?高中阶段学习的呈两性的氢氧化物为Al(OH)3
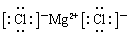 (3)表中元素形成的最强的碱为氢氧化钠其电子式为?; ①为N,其氢化物为氨气,电子式为
(3)表中元素形成的最强的碱为氢氧化钠其电子式为?; ①为N,其氢化物为氨气,电子式为 ;④和⑦所形成化合物是
;④和⑦所形成化合物是 电子式为:
电子式为:
(4) ⑦的单质是 ,⑩的单质是
,⑩的单质是 ,处于同一主族,非金属性逐渐降低,活泼性
,处于同一主族,非金属性逐渐降低,活泼性 大于
大于 ,
, 可以从溴的化合物的溶液中置换出溴单质,化学方程式为2NaBr+Cl2=2NaCl+Br2。
可以从溴的化合物的溶液中置换出溴单质,化学方程式为2NaBr+Cl2=2NaCl+Br2。
本题难度:一般
2、选择题 下列各组粒子中,具有相同的质子数和电子数的是(?)
A.OH一、F―、O2―、Ne
B.CH4、NH3、H2O、HF
C.NH4+、Na+、H3O+、PH4+
D.F一、O2一、Mg2+、A13+
参考答案:B
本题解析:A中质子数不同,B中质子数和电子数都是10个,C中质子数和电子数都不相同,D中质子数也是不同的,所以答案选B。
本题难度:一般
3、选择题 下列关于碱金属的叙述中不正确的是
A.碱金属单质在化学反应中表现出强还原性
B.Li 在氧气中燃烧主要生成Li2O2
C.碱金属离子的氧化性随着离子半径的增大而减小
D.随核电荷数的增加,单质与水反应剧烈程度增大
参考答案:B
本题解析:
答案:B
A、正确,碱金属最外层只有一个电子,单质在化学反应中表现出强还原性
B.不正确,Li 在氧气中燃烧主要生成Li2O
C.正确,碱金属离子的氧化性随着离子半径的增大而减小,原子半径大,对最外层电子的吸引力小;
D.正确,随核电荷数的增加,碱金属的金属性增强,单质与水反应剧烈程度增大
本题难度:一般
4、选择题 已知33As、35Br位于同一周期,下列关系正确的是 (? )
A.原子半径:As>C1>P
B.热稳定性:HC1>AsH3>HBr
C.还原性:As3->S2->C1-
D.酸性:H3AsO4>H2SO4>H3PO4
参考答案:C
本题解析:同一周期元素自左到右原子半径变小故A中C1>P错;同一周期元素自左到右非金属性增强,氢化物的稳定性增强故B中 AsH3>HBr错;非金属性越强最高价氧化物的水化物的酸性也越强,非金属性S>P>As,故D错
本题难度:一般
5、选择题 X、Y、Z是三种主族元素,如果Xm+与Yn-具有相同的电子层结构,Zn-半径大于Yn-半径,则三种元素的原子序数由大到小的顺序是
A.Z>X>Y
B.X>Y>Z
C.Z>Y>X
D.X>Z>Y
参考答案:A
本题解析:Xm+与Yn-具有相同的电子层结构,即离子核外电子总数相同,设X的原子序数为a,Y的原子序数为b,则可得:a―m=b+n,所以X的原子序数大于Y,C错;Zn-半径大于Yn-半径,即Z的原子序数大于Y的原子序数,B、D错;
正确选项为A;
本题难度:一般