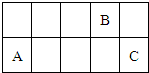
1���ƶ��� ���ֳ���Ԫ�ص����ʻ�ṹ��Ϣ���±����Ը�����Ϣ�ش��й����⡣

(1)д��Bԭ�ӵĵ����Ų�ʽ____________��
(2)AԪ�ص��⻯��ķе��ͬ��������Ԫ���⻯��е�________����ߡ��͡�������ԭ����____________________��
(3)DԪ�ص�ij��̬�����ӿ���KCN��Һ�γ�һ���׳ƻ�Ѫ�ε������ף��Ļ�ѧʽ�ɱ�ʾΪ
K4[D(CN)6]��������ԭ��D�Ļ��ϼ�Ϊ________������ˮ��Һ�еĵ��뷽��ʽΪ____________________����֪DԪ�ص���һ�ּ�̬�����ӿ���KCN��Һ�γ���һ��������ң��ҵ���λ�������ͬ�����ҵĻ�ѧʽΪ____________��
(4)���з��ӽṹͼ�еġ���ʾ�������Ԫ�ص�ԭ���г�ȥ�������ӵ�ʣ�ಿ�֣���o����ʾ��ԭ�ӣ�С�ڵ��ʾû���γɹ��ۼ����������ӣ����߱�ʾ���ۼ���
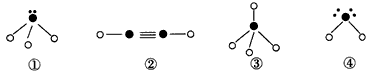
�������Ϸ����У�����ԭ��û�в���sp3�ӻ��γɻ�ѧ������________����д��ţ����ڢڵķ�������
____���Ҽ�
�ο��𰸣�(1)1s22s22p63s23p4
(2)�ߣ���ΪA���⻯����Ӽ�������
(3)+2��K4[Fe(CN)6]=4K++[Fe(CN)6]4-��K3[Fe(CN)6]
(4)�ڣ�3
���������
�����Ѷȣ�һ��
2��ѡ���� 13C-NMR(�˴Ź���)�����ں�̼������Ľṹ����14N��NMR�����ڲⶨ�����ʡ�������������ӵĿռ�ṹ�������й�13C��15N������ȷ����
A.13C��15N������ͬ��������
B.13C��C60��ͬһ������
C.15N��14N��Ϊͬλ��
D.15N�ĺ������������������ͬ
�ο��𰸣�C
�������������������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ������������Ϊ��������������֮����������������A��13C��15N���������ֱ���67��8��A����ȷ������һ����Ŀ���Ӻ�һ����Ŀ���ӵ�һ��ԭ���Ǻ��أ���13C��һ�ֺ��أ���C60��һ�ֵ��ʣ�B����ȷ����������ͬ����������ͬ��ͬһ��Ԫ�صIJ�ͬ���ػ���Ϊͬλ�أ�����ѡ��C��ȷ��15N�ĺ�����������������ֱ���7��8��D����ȷ����ѡA��
���㣺����ͬλ�ء������Լ�ԭ����ɵ��й��жϺͼ���
�����������ǻ���������Ŀ��飬���ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ�����ȷͬλ�ء����صĺ����Լ�ԭ����ɵı�ʾ����������������ü��ɡ�
�����Ѷȣ�����
3��ѡ���� �����й��������ʵıȽ���ȷ���ǣ�
A.�۵㡢�е㣺F2��Cl2��Br2��I2
B.���Ӱ뾶��F-��Na+��Mg2+��Al3+
C.���ԣ�LiOH��NaOH��KOH��RbOH
D.Na2CO3ˮ��Һ�У�c(Na+)��c(CO32-)��c(HCO3-)��c(OH-)��c(H+)
�ο��𰸣�B
���������
�����Ѷȣ�����
4��ѡ���� �����ڱ��й��ɽ���Ԫ�����ʵݱ���ɲ������ԣ��ɽ���ʡ�ԴӶ��õ�һ���µ����ڱ�������ǰ������Ԫ��A��B��C�������ڸ������ڱ��е����λ����ͼ������˵����ȷ���ǣ�������
A����Aԭ�ӵ������������ȵ��Ӳ�����1����C��һ�����������ʹƷ����Һ��ɫ
B����A�ĵ���������ˮ�Ҵ���Ӧ����B��������һ��Ϊ����������
C����A��������Ϊ�����������B������������ˮ����Ϊǿ��
D����A�������������ǿ�ᡢǿ�Ӧ�����⻯����۷е�C��B��