1、选择题 银器皿日久表面逐渐变黑,这是因为生成了Ag2S.有人设计用原电池原理除去银器表面的黑色.方法为:将其与Al片接触,一起浸泡在稀NaOH溶液中,放置一段时间后黑色褪去,取出用水洗净,恢复其原貌.总反应为2Al+3Ag2S+8OH-═2AlO
+6Ag+3S2-+4H2O
下列叙述不正确的是( )
A.反应后溶液的pH降低
B.溶液中的OH-离子向正极移动
C.负极的电极反应式为:2Al+8OH--6e-═2AlO+4H2O
D.正极的电极反应式为:3Ag2S+6e-=═6Ag+3S2-
参考答案:A.根据2Al+3Ag2S+8OH-═2AlO2-+6Ag+3S2-+4H2O知,氢氧根离子参加反应,所以氢离子浓度逐渐降低,溶液的pH逐渐减小,故A正确;
B.原电池放电时,氢氧根离子向负极移动,故B错误;
C.根据电池反应式知,负极上失电子发生氧化反应,所以发生的电池反应式为2Al+8OH--6e-═2AlO2-+4H2O,故C正确;
D.根据电池反应式知,正极上得电子发生还原反应,所以发生的电池反应式为3Ag2S+6e-=═6Ag+3S2-,故D正确;
故选B.
本题解析:
本题难度:简单
2、填空题 Ⅰ.短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X、Y、Z三种元素的质子数之和为
21。
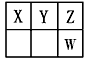
(1)写出W的简单离子的原子结构示意图________;氢元素与Z形成原子个数比为1∶1的化合物,其结构式为_________。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是
____________________ (用离子方程式表示) ;
(3)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式_______________,反应中每转移8mol 电子,消耗的还原剂质量为_________g。
(4)写出能说明Y的非金属性比Z弱的一个实验事实:____________________
Ⅱ.往1L体积不变的容器中加入0.200mol CO和1.00mol H2O(g),在t℃时反应:CO+ H2O(g)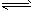 CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为________。
CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为________。
Ⅲ.甲醇燃料电池是一种相对理想的绿色能源,可用于电动汽车的电源;若该氢氧燃料电池以硫酸为电解质溶液,总反应为:2CH3OH + 3O2 = 2CO2+ 4H2O,则其正极的电极反应式_________________。
参考答案:Ⅰ(1)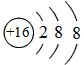 ;H-O-O-H;(2)NH4++H2O
;H-O-O-H;(2)NH4++H2O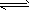 NH3·H2O+H+
NH3·H2O+H+
(3)C+4HNO3 CO2↑+4NO2↑+2H2O;24g;(4)O2比N2更容易与氢气化合(或H2O比NH3更稳定,其它合理答案也可以)
CO2↑+4NO2↑+2H2O;24g;(4)O2比N2更容易与氢气化合(或H2O比NH3更稳定,其它合理答案也可以)
Ⅱ 83.3%
Ⅲ O2 + 4H+ +4e- =2H2O
本题解析:
本题难度:一般
3、选择题 在下图所示的装置中,a为金属活动性顺序中氢前的金属,b为碳棒,关于此装置的各种叙述正确的是
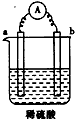
[? ]
A.碳棒上有气体放出,溶液酸性变弱
B.a是正极,b是负极
C.导线中有电子流动,电流从a极到b极
D.a极上发生了还原反应
参考答案:A
本题解析:
本题难度:简单
4、填空题 (8分)将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:
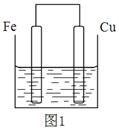
(以下均假设反应过程中溶液体积不变)。
⑴铁片上的电极反应式为?。
⑵铜片周围溶液会出现?的现象。
⑶若2 min后测得铁片和铜片之间的质量差为1.2g,计算:
①导线中流过的电子的物质的量为?mo1;
②该段时间内用硫酸铜表示的平均反应速率为?
参考答案:(1)Fe-2e-=Fe?2+;(2)溶液颜色变浅;(3)①0.02;② 0.01mol?L-1?min-1。
本题解析:(1)铁片、铜片和硫酸铜溶液构成原电池,铁较活泼,作原电池的负极,电极反应式为Fe-2e-=Fe?2+;(2)铜电极作原电池的正极,电极反应式为Cu2++2e-=Cu,铜离子浓度降低,则溶液颜色变浅;(3)①负极上铁溶解,正极上析出铜,铁片和铜片相差的质量为溶解铁和析出铜的质量之和,溶解铁的物质的量和析出铜的物质的量相等,设转移电子的物质的量为xmol,x/2×56+x/2×64=1.2,x=0.02;②硫酸铜的平均反应速率=0.01mol/(2min×0.5L)=0.01mol?L-1?min-1。
本题难度:一般
5、选择题 下列每组的三种物质中,两边的固体均有导线连接,插入中间的液体中,其中能组成原电池的是
[? ]
A.Zn | H2SO4(稀) | C
B.Cu | 酒精 | Ag
C.Zn | CCl4 | Cu
D.Fe | H2SO4(稀) | Fe
参考答案:A
本题解析:
本题难度:简单