1、填空题 (10分)熔融碳酸盐燃料电池(MCFS),发明于1889年。现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。
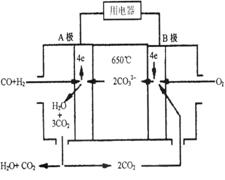
请回答下列问题:
(1)B极为_________极,发生_________(填“氧化”或“还原”)反应。
(2)电池总反应为___________________________________________。
(3)以此电源电解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为??g。
(4)电池中的电解质碳酸钠形成的水溶液体系不能用带玻璃塞的试剂瓶保存,其原因是?(用化学方程式表示)
2、填空题 甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
已知:
①?CH4(g)?+?H2O?(g)?=?CO?(g)+3H2?(g)?△H1=+206.2kJ・mol-1
②?CH4(g)+?1/2O2(g)=CO(g)+2H2(g)?△H2=-35.4?kJ・mol-1
③?CH4(g)?+?2H2O?(g)?=CO2(g)?+4H2(g)?△H3=+165.0?kJ・mol-1
(1)CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为__________________。 ?
(2)从原料选择和能源利用角度,比较方法①和②,为合成甲醇,用甲烷制合成气的适宜方法为________(填序号),其原因是__________________________。
(3)合成气中的H2可用于生产NH3,在进入合成塔前常用Cu(NH3)2Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:Cu(NH3)2Ac?+?CO?+?NH3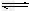 [Cu(NH3)3]Ac・CO?△H<0 Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是______________。
[Cu(NH3)3]Ac・CO?△H<0 Cu(NH3)2Ac溶液吸收CO的适宜生产条件应是______________。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。
①?0<V≤44.8?L时,电池总反应方程式为___________________; ?
②?44.8?LV≤89.6?L时,负极电极反应为_____________; ?
③?V=67.2?L时,溶液中离子浓度大小关系为__________________。
3、简答题 (1)写出以石墨为电极,H2、O2、Na2SO4溶液构成的燃料电池的电极反应式:负极:______;正极:______
(2)写出以石墨为电极,H2、O2、H2SO4溶液构成的燃料电池的电极反应式:负极:______;正极:______
(3)写出以石墨为电极,H2、O2、NaOH溶液构成的燃料电池的电极反应式:负极:______;正极:______.
4、填空题 (5分)21世纪最富有挑战性的课题之一是使汽油氧化直接产生电流,新研制的某汽油燃料电池的一个电极通入空气,另一个电极通入汽油蒸气,填写下列空格。
(1)汽油燃料电池的能量转换形式是将________能直接转化为______能。
(2)通入空气的那个电极是燃料电池_________极(选填“正”或“负” )该电极上若有
32g O2参加反应,则反应过程中转移了_________mol e-
5、选择题 某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料。下列说法正确的是
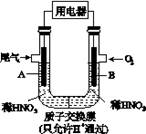
A.电极A表面反应之一为NO2-e-+H2O==NO3-+2H+
B.电极B附近的c(NO3-)增大
C.电解质溶液中电流的方向由B到A,电子的流向与之相反
D.该电池工作时,每转移4 mol电子,生成22.4 L O2