1、选择题
A.0.12 mol
B.0.11 mol
C.0.09 mol
D.0.08 mol
参考答案:B
本题解析:铜与HNO3反应时,消耗的HNO3进入Cu(NO3)2和氮的氧化物(NO2或NO)。n(Cu)=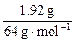 =0.03 mol;n(气体)=
=0.03 mol;n(气体)=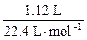 =0.05 mol;所以共耗HNO3的物质的量n(HNO3)=0.03 mol×2+0.05 mol=0.11 mol。
=0.05 mol;所以共耗HNO3的物质的量n(HNO3)=0.03 mol×2+0.05 mol=0.11 mol。
本题难度:简单
2、选择题 将盛有12mL NO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是
A.1.2mL
B.2.4mL
C.3.6mL
D.4.8mL
参考答案:A
本题解析:考查NO2溶于水的有关计算。如果剩余气体是氧气,则根据反应式4NO2+O2+2H2O=4HNO3可知,参加反应的气体一共是10ml,则其中氧气是2mol,所以氧气一共是4ml。如果剩余气体是NO,则反应中剩余NO2,剩余的NO2继续和水反应,方程式为3NO+H2O=2HNO3+NO,所以剩余的NO2水6mol,则参加反应的气体是12ml-6ml=6ml。其中氧气是6ml÷5=1.2ml,答案选A。
本题难度:困难
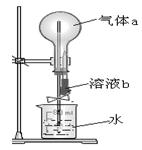
3、选择题 如图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成“喷泉”的组合是