1��ѡ���� �����Ϊ1��2��3����ɵ�N2��O2��CO2�������100g�ڱ�״�������Ϊ
A.60L
B.30L
C.11.2L
D.112L
�ο��𰸣�A
������������������֮�ȵ������ʵ���֮�ȣ���������ʵ���Ϊxmol��������Ϊ2xmol��������̼Ϊ3xmol�����ݻ�����������������x��ֵ���ٸ���V=nVm�����������״���������
������֮�ȵ������ʵ���֮�ȣ���������ʵ���Ϊxmol��������Ϊ2xmol��������̼Ϊ3xmol�����ԣ�
xmol��28g/mol+2xmol��32g/mol+3xmol��44g/mol=100g��
��ã�x=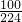 mol��
mol��
���Ա�״���£������������Ϊ��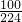 mol+2��
mol+2��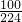 mol+3��
mol+3��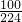 mol����22.4L/mol=60L��
mol����22.4L/mol=60L��
��ѡ��A��
���������鰢��٤�����ɼ����۵��йؼ��㣬�Ѷ��еȣ��ؼ��������֮���ж����ʵ�����ϵ��
�����Ѷȣ�����
2��ѡ���� ��NA��ʾ�����ӵ�������������������ȷ���ǣ�������
A��1?molCl2�μӷ�Ӧת�Ƶ�����һ��Ϊ2NA
B��7.8?g?Na2O2�к��е���������Ϊ0.1NA
C��25��ʱ��pH=14?Ba��OH��2��Һ1L��Ba2+��ΪNA
D����״���£�11.2?L?CO2�к����õ��Ӷ���ΪNA
�ο��𰸣�A��1?molCl2�μӷ�Ӧת�Ƶ���������Ϊ2NA����������������Ӧ��Ҳ����ΪNA�����������������Ʒ�Ӧ����A����
B��7.8?g?Na2O2���ʵ���Ϊ0.1mol���������ӹ���������0.1mol����B��ȷ��
C��pH=14?Ba��OH��2��Һ1L������������Ũ��Ϊ1mol/L�����ʵ���Ϊ1mol��Ba2+��Ϊ0.5NA����C����
D����״���£�11.2?L?CO2���ʵ���Ϊ0.5mol��1��CO2�����к�4�Թ��õ��Ӷԣ�����0.5molCO2�����õ��Ӷ�2mol����D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ��NAΪ�����ӵ���������ֵ������˵���������
[? ]
A��NA��Fe(OH)3�������ӵ�����Ϊ107g
B��0.1 mol����0.1 mol Cl2�г��ȼ�գ�ת�Ƶĵ�����Ϊ0.2 NA
C��24 g NaH��������������������Ϊ2NA
D����״���£�22.4 LCO2��O2��������к��е���ԭ����Ϊ2NA
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� ��NA��ʾ�����ӵ�������ֵ������������ȷ����
[? ]
A��0.1molPCl3���γɹ��ۼ��ĵ�������0.3NA
B�����³�ѹ�£�1.6g?O2?��O3?�����������������Ϊ0.8?NA
C��һ�������£�2mol?SO2?��?1mol?O2?������Ӧ��ת�Ƶĵ�������һ����4NA
D��1L?0.1mol��L-1����������Һ�з�������Ϊ0.1?NA
�ο��𰸣�B
���������
�����Ѷȣ���
5��ѡ���� ��NA��ʾ�����ӵ����������������в���ȷ���ǣ�������
A��ͨ��״���£�1molSO3���еķ�����ΪNA��
B��1molOH-�����⣬�ṩ�ĵ�����ĿΪNA��
C����״���£���NA���ԭ�ӵ�������ԼΪ22.4L
D����״���£�VLˮ���е���ԭ�Ӹ���ԼΪ
NA
�ο��𰸣�A��ÿĦ�����ʺ�NA��������A��ȷ��
B�����ʱ��OH-ʧ���ӵĵ缫��ӦʽΪ��4OH--4e-�TO2��+2H2O����1molOH-�����⣬�ṩ�ĵ�����ĿΪNA������B��ȷ��
C����״���£�����Ħ�����Ϊ22.4L/mol���Ϊ��ԭ�ӷ��ӣ����Ժ�NA���ԭ�ӵ�������ԼΪ22.4 L����C��ȷ��
D������£�ˮΪҺ̬������V Lˮ�����ʵ�������V22.4mol���ʺ��е���ԭ�Ӹ�������V22.4NA����D����ȷ��
��ѡD��
���������
�����Ѷȣ�һ��