1��ʵ���� ������������������ͭ���Ǻ�ɫ��ĩ�����������ϡ�ijУһ��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ��Fe2O3��Cu2O������
̽���������£� ?
[��������]Cu2O��һ�ּ������������ϡ��������Cu��CuSO4���ڿ����м�������CuO
[�������] ?
����1����ɫ��ĩ��Fe2O3�� ?
����2����ɫ��ĩ��Cu2O ?
����3����ɫ��ĩ��Fe2O3����Cu2O�Ļ���� ?
[���̽��ʵ��] ȡ������ĩ������ϡ�����У���������Һ���ٵμ�KSCN�Լ��� ?
(1)������l��������ʵ��������______________________��
(2)���μ�KSCN�Լ�����Һ�����ɫ����֤��ԭ�����ĩ��һ����������������������Ϊ����˵��������?________�������������(����д����Ӧ�ķ���ʽ) _______________��
(3)�������ĩ��ȫ�ܽ�������ڣ��μ�KSCN�Լ�ʱ��Һ�����ɫ����֤��ԭ�����ĩ��_____________�� ?
[̽������]��ʵ�������ȷ����ɫ��ĩΪFe2O3��Cu2O�Ļ���
(4)ʵ��С�����ü��ȷ��ⶨCu2O������������ȡa?g�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊb?g(?b>a)����������Cu2O����������Ϊ________________��
�ο��𰸣�(1)������ȫ�ܽ⣬��Һ�ʺ�ɫ
(2)����������ԭ�����ĩΪFe2O3��Cu2O�Ļ����ʱ������ϡ����������Fe3+ȫ����Cu��Ӧ����Fe2+���μ�KSCN��Һ��Ҳ���ɫ
(3)Fe2O3��Cu2O?
(4)[9(b-a)��/a?]?��100%?��?[144?(b-a)��/16?a]��100
���������
�����Ѷȣ�һ��
2��ѡ���� ������Һ��һ�ֳ��õ�ֲ��ɱ��������������ͭ����ʯ�ҡ�ˮ��һ���ı������ƶ��ɣ���һ������ɫ��״����Һ�塣ͨ���������䣬����Ϊ��������������������ʢװ������Һ(����)��
A����������
B��ͭ������
C����������
D������
�ο��𰸣�C
������������Ľ����Ա�ͭǿ�������û���ͭ��Cu2����Fe=Fe2����Cu��
�����Ѷȣ���
3������� ���Ȼ�������ѧ��ѧʵ�����г��õĻ�ѧ�Լ���ijͬѧ���÷���м��������ͭ�Ȳ������ᷴӦ�����ʣ����Ʊ�FeCl3?6H2O����ͬѧ��Ƶ�ʵ��װ����ͼ��ʾ����ʵ�鲽�����£�A�з��з���м���ձ���ʢ�й�����ϡ���ᣬʵ��ʱ��a���ر�b���ӷ�Һ©������A�мӹ��������ᣬ��ʱ��Һ��dz��ɫ���ٴ�b���й��ˣ����˽�����ȡ�ձ�����Һ������������ȣ�����������ˮ��ʹʣ��HNO3�ֽ⣬�ٽ��½ᾧ��FeCl3?6H2O���壮��д���пհף�
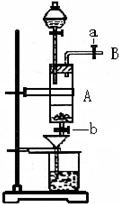
��1���ռ�����B��������ɲ��õķ�����______���μ�����ʱ�����ַ�Ӧ���ʽ�֮�����봿���۷�ӦҪ�죬��ԭ����______��
��2���ձ��ڷŹ���ϡHNO3��ԭ����______��������Ӧ�����ӷ���ʽ��______��
��3������ʵ������У����ɼ�a���������Ϊ�ų������������⣬��һ��Ŀ����______��
��4�����ձ�����Һ��������Ũ�����ٽ��½ᾧ���Ƶ�FeCl3?6H2O��������ֱ�����ɵķ������Ƶþ����������______
��5������Ϊ��ʵ����ڵ�ȱ������У�______��
�ο��𰸣���1������B��������Ϊ�����������ܶȱȿ���С�Ҳ�����ˮ��������ˮ���������ſ������ռ���Cu�����γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죬
�ʴ�Ϊ������ˮ���������ſ������������м�к�����Cu�����ʣ��γ�Fe-Cuԭ���ʹ��Ӧ���ʼӿ죻
��2��������ϡHNO3��֤ʹFe2+ ȫ��������Fe3+����Ӧ�����ӷ���ʽ��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
�ʴ�Ϊ��ϡHNO3��ǿ�����ԣ�Ϊ��֤ʹFe2+ȫ��������Fe3+��3Fe2++4H++NO3-�T3Fe3++NO��+2H2O��
��3��ʹ��Һ©���е���ɵ���A�У��ʴ�Ϊ���������ͨ��ʹ��Һ©���е���ɵ���A�У�
��4����ΪFeCl3��ǿ��������ˮ�⣬��������ʱʹHCl�ӷ����ˮ��ƽ�����ƣ���˵ò���FeCl3?6H2O��
�ʴ�Ϊ����ΪFeCl3��ǿ��������ˮFeCl3+3H2O?Fe��OH��3+3HCl����������ʱʹHCl�ӷ����ˮ��ƽ�����ƣ���˵ò���FeCl3?6H2O��
��5����β������װ�ã���ϡHNO3����FeCl2ʱ���������������ʹ�Ƶõ�FeCl3?6H2O������
�ʴ�Ϊ����Ӧ�в������к��������Ⱦ��������ϡHNO3����FeCl2ʱ����Fe��NO3��3���ɶ�ʹ�Ƶõ�FeCl3?6H2O������
���������
�����Ѷȣ�һ��
4��ѡ���� ����������;������ȡ��ͬ����������ͭ����ͭ��Ũ���ᷴӦ����ͭ��ϡ���ᷴӦ����ͭ��������Ӧ����CuO��CuO����ϡ���ᷴӦ�������й���������ȷ����?��������
A�������ĵ�����������٣��ڣ���
B���Ի�����ɵ�Σ��������С
C����ͭ��Ũ����������죬����ȡ����ͭ����ѷ����Ǣ�
D������;�������ĵ�ͭ���������
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
5��ѡ���� ���ֽ�����ĩ�Ļ����15 g��Ͷ��������ϡ�����У��õ�5.6 L��������״�����������ֻ��������ǣ�?��
A��þ����
B��þ����
C������п
D���ƺ�þ
�ο��𰸣�C
���������������ĩͶ��������ϡ�����У��ų�����������ʧ���ӣ����е������ӣ�H+���õ��ӡ���������ԭ��Ӧ�Ĺ���֪������ʧ�����������������ӣ�H+���õ�����������֪��15 g���������ʧ���ӵ����ʵ���Ϊ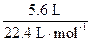 ��2="0.5" mol������������ƽ��Ħ����������Ϊ15 g/0.5 mol="30" g�� mol-1������ѡ��Ľ�����Ħ�����������ֱ�Ϊ��þ��24 g/2 mol="12" g�� mol-1������56 g/2 mol="28" g�� mol-1������27g/3 mol="9" g�� mol��1��п��65 g/2 mol="32.5" g�� mol��1���ƣ�23 g�� mol��1����ƽ��ֵ������֪������п�������⡣
��2="0.5" mol������������ƽ��Ħ����������Ϊ15 g/0.5 mol="30" g�� mol-1������ѡ��Ľ�����Ħ�����������ֱ�Ϊ��þ��24 g/2 mol="12" g�� mol-1������56 g/2 mol="28" g�� mol-1������27g/3 mol="9" g�� mol��1��п��65 g/2 mol="32.5" g�� mol��1���ƣ�23 g�� mol��1����ƽ��ֵ������֪������п�������⡣
�����Ѷȣ�һ��