1��ѡ���� ij�о�С����ʵ�������ؾ�ʯ(��Ҫ�ɷ�BaSO4)�Թ�ҵ����BaS����ģ��ʵ�顣BaS�ǿ����Σ��ڹ�ҵ�����У������Ʊ��������ε��м�����֪��
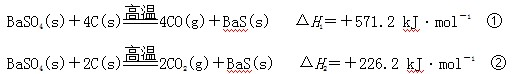
����˵������ȷ����
A��������Ӧ��BaSO4����������
B����ӦC(g)��CO2(g) 2CO(g)�Ħ�H3>��172.5 kJ��mol��1
2CO(g)�Ħ�H3>��172.5 kJ��mol��1
C��ʵ�������б�����������̿ʹBaSO4�õ���ֵĻ�ԭ��ͬʱ��Ҫͨ���������Ϊ�٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ�������
D����BaS��Ϊ������������Ǧ��������ת��
�ο��𰸣�B
���������������Ӧ����Ļ��ϼ۾����ͣ�A����ȷ�����ݸ�˹���ɣ�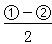 �Ȼ�ѧ����ʽC(s)��CO2(g)
�Ȼ�ѧ����ʽC(s)��CO2(g) 2CO(g) ��H����172.5 kJ��mol��1����̬̼����ת��ɹ�̬̼������ų��������ʷ�ӦC(g)��CO2(g)
2CO(g) ��H����172.5 kJ��mol��1����̬̼����ת��ɹ�̬̼������ų��������ʷ�ӦC(g)��CO2(g) 2CO(g)�Ħ�H3<��172.5 kJ��mol��1��B�����
2CO(g)�Ħ�H3<��172.5 kJ��mol��1��B�����
�����Ѷȣ�һ��
2��ѡ���� ��֪��Ӧ��A+2B=2C+3D��һ�����ȷ�Ӧ��������˵������ȷ���ǣ�������
A��A��������C��������
B���÷�Ӧһ��Ҫ���Ȳ��ܷ���
C����Ӧ��������ܺͱ�������������ܺ�С
D����Ӧ�жϼ�ʱ���յ��������γɻ�ѧ��ʱ�ų���������
�ο��𰸣�A��A+2B=2C+3D��һ�����ȷ�Ӧ��˵����Ӧ������������������������������˵��A��������C�������Ĺ�ϵ����A����
B�����ȷ�Ӧ��һ���ڼ��ȵ������·����������Ȼ�狀�ʮˮ�����������ķ�Ӧ�������ȷ�Ӧ�����Dz����������ܷ�������B����
C������Ӧ��������������������������ʱ����Ӧ�����ȷ�Ӧ����C��ȷ��
D������Ӧ�жϼ�ʱ���յ��������γɻ�ѧ��ʱ�ų���������ʱ����Ӧ�����ȷ�Ӧ����D����
��ѡC��
���������
�����Ѷȣ�һ��
3������� ��15�֣��������糧�ͷų������������NOx����SO2��CO2���������ɻ������⡣��ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
��1�����������ü������ԭNOx��
CH4(g) �� 4NO2(g) ��4NO(g) �� CO2(g) �� 2H2O(g)?��H1����574 kJ��mol��1
CH4(g) �� 4NO(g) ��2N2(g) �� CO2(g) �� 2H2O(g)?��H2����1160 kJ��mol��1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ?��
��2����̼����CO2ת��Ϊ�״���CO2(g)��3H2(g) CH3OH(g)��H2O(g)?��H3
CH3OH(g)��H2O(g)?��H3
 ?
?
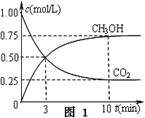
����һ���º����ܱ������г���1 mol CO2��3 mol H2����������Ӧ�����CO2��CH3OH(g)Ũ����ʱ��仯��ͼ1��ʾ���ش�0~10 min�ڣ�������ƽ����Ӧ����Ϊ?mol/(L��min)����10 min�����¶Ȳ��䣬����ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)����ƽ��?������������������ƶ���
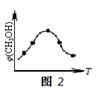
��ȡ��ݵ������CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״�����������գ�CH3OH���뷴Ӧ�¶�T�Ĺ�ϵ������ͼ2��ʾ��������CO2ת��Ϊ�״��ķ�Ӧ�ġ�H3?0�����������������������
��3����������Na2SO3��Һ���ѳ������е�SO2��Na2SO3����NaOH��Һ����SO2�Ƶá�NaOH��Һ����SO2�Ĺ����У�pH��n(SO32-)�Un(HSO3��)�仯��ϵ���±���
n(SO32��)�Un(HSO3��)
| 91�U9
| 1�U1
| 9�U91
|
pH
| 8.2
| 7.2
| 6.2
|
�� ���ϱ��жϣ�NaHSO3��Һ���������ԣ��û�ѧƽ��ԭ�����ͣ���������������������?������
�� ����Һ������ʱ������Ũ�ȹ�ϵ��ȷ���ǣ�ѡ����ĸ��������������
a��c(Na+)=2c(SO32-)+c(HSO3-)
b��c(Na+) > c(HSO3-) > c(SO32-) > c(H+) = c(OH-)
c��c(Na+) + c(H+) = c(SO32-) + c(HSO3-) + c(OH-)
�ο��𰸣�(15��)
��1��CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=-867?kJ?mol-1��3�֣�
��2����0.225?��2�֣�������2�֣�
�ڣ���2�֣�
��3�����ᣨ2�֣���Һ�д��ڣ�HSO3- SO32-�� H+?HSO3-��H2O
SO32-�� H+?HSO3-��H2O H2SO3��OH-����̶ȴ���ˮ��̶ȣ�����Һ�����ԣ�2�֣�
H2SO3��OH-����̶ȴ���ˮ��̶ȣ�����Һ�����ԣ�2�֣�
��ab��2�֣�
�����������1������д��CH4��NO2��ԭΪN2�Ļ�ѧ����ʽ��ע��״̬��Ȼ����ݸ�˹��������ʱ䣬��1����Ӧ����NO2����2����Ӧ����N2�ɵã�?H=1/2?H1+1/2?H2=-867?kJ?mol-1������д���Ȼ�ѧ����ʽ��
��2����0~10 min�ڣ�������ƽ����Ӧ����v��H2��=3v��CH3OH��="3��0.75mol/L��10min=0.225" mol/��L��min����
��������ʽ���������ƽ��Ũ�ȣ�CO2��g����3H2��g�� CH3OH��g����H2O��g��
CH3OH��g����H2O��g��
��ʼŨ�ȣ�mol?L?1��? 1.00? 3?0?0
ת��Ũ�ȣ�mol?L?1��? 0.75? 2.25? 0.75? 0.75?
ƽ��Ũ�ȣ�mol?L?1��? 0.25? 0.75?0.75? 0.75
ƽ�ⳣ��K=0.75��0.75�£�0.25��0.753��=5.33������ܱ��������ٳ���1 mol CO2(g)��1 mol H2O(g)��Ũ����Q=0.75��1.75�£�1.25��0.753��="2.49" < K����ƽ�������ƶ���
����ͼ��֪��ߵ㷴Ӧ����ƽ�⣬��ƽ����¶�Խ�ߣ��գ�CH3OH��ԽС��ƽ�����淴Ӧ���У������¶�ƽ�����ȷ�����У��淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ������H3��0��
��3�����ɱ����е����ݿ�֪��HSO3-Խ�࣬����Խǿ������NaHSO3��Һ�����ԣ�HSO3?�������������ӣ����뷽��ʽΪHSO3-?H++SO32-��ͬʱHSO3?����ˮ�⣬HSO3-��H2O H2SO3��OH-����Һ��������������������ˮ�⡣
H2SO3��OH-����Һ��������������������ˮ�⡣
�ڵ���Һ������ʱ������Ϊ�������ƺ����������ƣ�������ˮ��ij̶���ȣ�a���ɵ���غ��֪��c��H+��+c��Na+���T2c��SO32-��+c��HSO3-��+c��OH-����������Һ��c��H+���Tc��OH-������c��Na+���T2c��SO32-��+c��HSO3-������ȷ��b��SO32-+H2O?HSO3-+OH-��HSO3-?H++SO32-������������ˮ�⣬������Ũ��Ϊc��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-������ȷ��c�����ݵ���غ�ɵã�c��Na+��+c��H+���T2c��SO32-��+c��HSO3-��+c��OH-��������
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ���ǣ�?��
A����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
B����Ӧ�Ƿ��Ȼ��������ɷ�Ӧ��������������������Դ�С����
C�����������仯�����ʱ仯���ǻ�ѧ�仯
D�����ȷ�Ӧ�ڳ�����һ��������
�ο��𰸣�B
�����������Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ���뷴Ӧ������ϵ��ֻ�뷴Ӧ�������������������Դ�С�й�ϵ������ѡ��A��D����ȷ��B��ȷ�������仯������Ҳ���������ı仯��C����ȷ����ѡB��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Է�Ӧ�Ⱥ����Լ�Ӱ�����ص��˽���������ڹ���ѧ���Ļ���֪ʶ�����ѧ����Ӧ������������������ѧ���������������ͷ�ɢ˼ά��������������Ҫע����������仯�е���ЧӦ�����Ƿ��ȷ�Ӧ�����ȷ�Ӧ��
�����Ѷȣ�һ��
5��ѡ���� ��֪250C��101KPa�£���C(s)+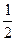 O2(g)="CO(g)?" ��H=
O2(g)="CO(g)?" ��H= 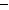 Q1kJ/mol?��2 CO(g)+ O2(g)=2CO2(g)?��H=
Q1kJ/mol?��2 CO(g)+ O2(g)=2CO2(g)?��H=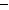 Q2kJ/mol ��Q1��Q2��Ϊ�������ݴ��ƶϣ�����˵����ȷ����
Q2kJ/mol ��Q1��Q2��Ϊ�������ݴ��ƶϣ�����˵����ȷ����
A��̼��ȼ����ΪQ1kJ/mol
B��2molCO(g)�����е�����һ������2molCO2(g)�����е�����
C��һ��������̼ȼ�գ�����CO2(g)������ CO(g)ʱ�ų���������
D��̼ȼ������CO2������Ȼ�ѧ����ʽΪ��C(s)+ O2(g)=CO2(g) ��H= 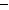 ��Q1+Q2��kJ/mol
��Q1+Q2��kJ/mol
�ο��𰸣�
C
���������
A�ȼ������ָ1mol������ȫȼ�գ������ȶ��Ļ�������ų�������������C(s)+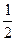 O2(g)="CO(g)?" ��H=
O2(g)="CO(g)?" ��H= 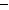 Q1kJ/mol�����ɵ���CO�������ȶ��Ļ��������Q1kJ/mol����̼��ȼ���ȣ�B���Ӧ�����ڷ��ȷ�Ӧ��ֻ��˵2molCO(g)��1molO2(g)�����е�����һ������2molCO2(g)�����е�������C�����CO2(g)����ȫȼ�գ������� CO(g)���Dz���ȫȼ�գ�����ǰ�߷ų��������ࣻD���H=
Q1kJ/mol�����ɵ���CO�������ȶ��Ļ��������Q1kJ/mol����̼��ȼ���ȣ�B���Ӧ�����ڷ��ȷ�Ӧ��ֻ��˵2molCO(g)��1molO2(g)�����е�����һ������2molCO2(g)�����е�������C�����CO2(g)����ȫȼ�գ������� CO(g)���Dz���ȫȼ�գ�����ǰ�߷ų��������ࣻD���H= 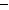 ��2Q1+Q2��kJ/mol
��2Q1+Q2��kJ/mol
�����Ѷȣ�һ��