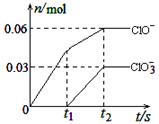
1、选择题 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列说法正确的是
A.苛性钾溶液中KOH的物质的量是0.09mol
B.ClO3-的生成是由于氯气的量的多少引起的
C.在酸性条件下ClO-和ClO3-可生成Cl2
D.反应中转移电子的物质的量是0.21mol
参考答案:D
本题解析:根据图像可知反应后,生成KClO和KClO3分别是0.06mol和0.03mol,则根据电子的都是守恒可知,生成氯化钾是0.06mol×1+0.03mol×5=0.21mol。所以D正确,A不正确,应该是0.3mol。B不正确,应该和温度有关系;C不正确,两种离子不可能都得到电子,答案选D。
本题难度:一般
2、选择题 下列有关化工生产和物质的性质应用,说法正确的是( )
A.生产玻璃和水泥都要用到的原料是石灰石和黏土
B.工业上金属Na、Mg、Al都是用电解熔融的氯化物制得的
C.食盐、Br2、Mg(OH)2都可以从海水中提取
D.氯气、漂白粉、明矾都可以用于自来水的消毒
参考答案:A.生产玻璃用到的原料是石灰石、纯碱、石英;生产水泥用到的原料是石灰石、粘土等,所以生产两种物质都需要石灰石,故A错误;
B.工业上生产钠、镁采用电解其熔融盐的方法,用电解熔融氧化铝的方法冶炼铝,故B错误;
C.海水中含有Mg2+、Na+、Cl-、Br-等,所以可以从海水中提取食盐、Br2、Mg(OH)2,故C正确;
D.氯气和漂白粉都具有强氧化性,能杀菌消毒,明矾没有强氧化性,明矾水解生成的氢氧化铝胶体具有吸附性,能吸附悬浮物而净水,故D错误;
故选C.
本题解析:
本题难度:简单
3、选择题 红色花瓣遇到新制氯水,颜色变化叙述正确的是
A.褪色
B.不变色
C.颜色加深
D.变蓝色
参考答案:A
本题解析:新制氯水检验漂白性,所以红色花瓣遇到新制氯水,颜色变化是褪色,答案选A。
点评:该题是高考中的常见题型,试题贴近生活,有助于调动学生的学习兴趣和学习积极性。该题主要是考查学生对氯水漂白性的熟悉掌握程度以及灵活运用基础知识解决实际问题的能力。
本题难度:简单
4、选择题 下列各物质中,既能通过金属与氯气反应,又能通过金属与盐酸反应制得的是
A.MgCl2
B.FeCl2
C.FeCl3
D.CuCl2
参考答案:A
本题解析:略
本题难度:简单
5、选择题 如图是一套检验气体性质的实验装置,向装置中缓慢通入气体X,若关闭活塞S,则品红试液无变化,而澄清石灰水变浑浊;若打开活塞S,则品红试液褪色。据此判断气体X和洗瓶内的液体Y可能是

?
| A
| B
| C
| D
|
X
| Cl2
| SO2
| CO2
| NH3
|
Y
| 饱和NaHSO3溶液
| 饱和NaHCO3溶液
| Na2SO3溶液
| 浓H2SO4
|
?
参考答案:B
本题解析:根据题意气体X能使品红试液褪色,CO2、NH3不能使品红试液褪色,排除C、D;液体Y 能吸收气体X且产生使澄清石灰水变浑浊的气体,排除A;SO2与饱和NaHCO3溶液反应生成CO2,能使澄清石灰水变浑浊,选B.
本题难度:一般