1、实验题 【化学-选修化学与技术】(15分)
美国科学家理查德-海克和日本科学家根岸英一、铃木彰因在研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖。有机合成常用的钯/活性炭催化剂,长期使用催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收。一种由废催化剂制取氯化钯的工艺流程如下:
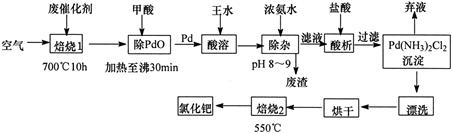
(1)废钯催化剂经烘干后,再在700℃的高温下焙烧,焙烧过程中需通入足量空气的原因是________;甲酸还原氧化钯的化学方程式为________。
(2)钯在王水(浓硝酸与浓盐酸按体积比1∶3)中转化为H2PdCl4,硝酸还原为NO,该反应的化学方程式为:____________。
(3)钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如下图1~图3所示,则王水溶解钯精渣的适宜条件(温度、时间和王水用量)为________、________、________。

(4)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+?,此时铁的存在形式是________(写化学式)。
(5)700℃焙烧1的目的是:________;550℃焙烧2的目的是:________。
参考答案:(1)使活性炭充分燃烧而除去(2分)PdO+HCOOH=Pd+CO2+H2O(2分)
(2)3Pd+12HCl+2HNO3=3H2PdCl4+2NO+4H2O(2分)
(3)80~90OC(或90oC左右)、反应时间约为8h、钯精渣与王水的质量比为1:8(3分)
(4)Fe(OH)3(2分)
(5)除去活性炭及有机物(2分);脱氨(将Pd(NH3)2Cl2转变为PdCl2)(2分)
本题解析:(1)由于废钯催化剂中含有活性炭,在高温下需要通过氧气将其氧化生成CO2而除去。甲酸还原氧化钯的氧化产物水是CO2,所以化学方程式为
PdO+HCOOH=Pd+CO2+H2O。
(2)根据所给的反应物和生成物可写出该反应的方程式,即
3Pd+12HCl+2HNO3=3H2PdCl4+2NO+4H2O。
(3)根据图中信息可知,最适宜的体积应该是80~90OC(或90oC左右)、反应时间约为8h、钯精渣与王水的质量比为1:8。
(4)在碱性溶液中,铁离子生成氢氧化碳沉淀而析出。
(5)700℃焙烧1的目的是除去活性炭及有机物。由于沉淀中含有氨气,所以灼烧的目的是将Pd(NH3)2Cl2转变为PdCl2。
本题难度:一般
2、简答题 已知反应:
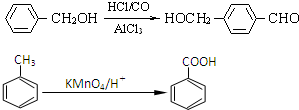
现有物质A~I的转化关系如下图:
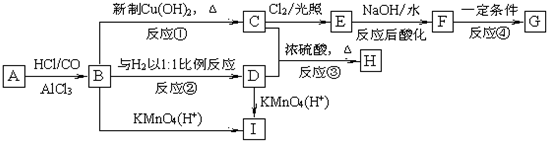
若B的分子式为C8H8O,其苯环上的一元取代物只有两种;G为高分子化合物.请回答下列问题:
(1)写出下列反应的反应类型:反应①______,反应③______.
(2)写出下列物质的结构简式:F______,I______,A______.
(3)写出下列反应的化学方程式:
①B→C:______;
②C+D→H:______;
③F→G:______;
(4)C的同分异构体且属于酯类的芳香族化合物共有______种,请写出其中一种同分异构体的结构简式:______.
参考答案:B的分子式为C8H8O,由A发生信息反应生成,B不饱和度=8×2+2-82=5,其苯环上的一元取代物只有两种,则侧链含有双键,应为2个侧链处于对位,结合反应信息可知,B为 、则A为
、则A为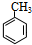 .B在新制氢氧化铜、加热条件下氧化生成C,则C为
.B在新制氢氧化铜、加热条件下氧化生成C,则C为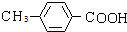 ,B与氢气1:1发生加成反应生成D,则D为
,B与氢气1:1发生加成反应生成D,则D为 ,B被酸性高锰酸钾氧化生成I,D氧化也生成I,结合反应信息可知,I为
,B被酸性高锰酸钾氧化生成I,D氧化也生成I,结合反应信息可知,I为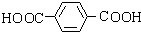 .C与D在浓硫酸、加热条件下发生酯化反应生成H,则H为
.C与D在浓硫酸、加热条件下发生酯化反应生成H,则H为 .
.
C光照发生甲基中取代反应生成E,E在氢氧化钠水溶液、加热条件发生水解反应,并酸化生成F,F生成G为高分子化合物,则F中含有-OH、-COOH,则C发生一氯取代生成E,则E为 ,故F为
,故F为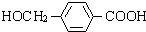 ,F发生缩聚反应生成G,则G为
,F发生缩聚反应生成G,则G为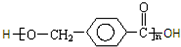 ,
,
(1)反应①属于氧化反应;反应③属于酯化反应,
故答案为:氧化反应;酯化反应;
(2)由上述分析可知,F为 ,I为
,I为 ,A为
,A为 ,
,
故答案为: ;
; ;
; ;
;
(3)①B→C反应方程式为: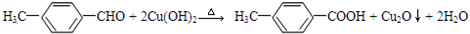 ;
;
②C+D→H反应方程式为: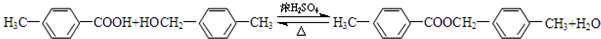 ;
;
③F→G反应方程式为: ,
,
故答案为: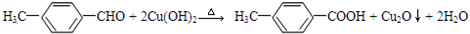 ;
;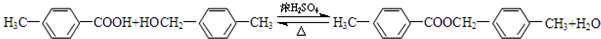 ;
; ;
;
(4)C的同分异构体且属于酯类的芳香族化合物的同分异构体的结构简式有: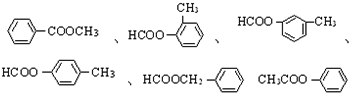 ,共有6种,
,共有6种,
故答案为:6; 中任意一种.
中任意一种.
本题解析:
本题难度:一般
3、简答题 分子式为C3H6O2的二元混合物,如果在1H-NMR谱上观察到氢原子给出的峰有两种情况:第一种情况强度是3:3;第二种情况强度是3:2:1.由此可推断混合物中其中一种有机物是(都写结构简式)______;另一种有机物是______或______或______.
参考答案:混合物是由分子式为C3H6O2的两种有机物混合而成,由各类有机物的通式可初步判断该有机物可能是饱和一元羧酸、酯或含羟基的醛或酮.第一种有机物的1H-NMR谱中有两组信号峰且强度是3:3,则此中有两种不等性氢原子,每种都有三个等性氢原子,由此得出结构简式为CH3COOCH3.另一种有机物1H-NMR谱中有三组信号峰,强度之比为3:2:1,说明此有机物中有三种不等性氢原子,且个数比为3:2:1,由此推测其结构中含有-CH3、-CH2-、-OH或-CHO等基团,所以结构简式为CH3CH2COOH、CH3COCH2OH、HCOOCH2CH3等.
故答案为:CH3COOCH3;CH3CH2COOH;CH3COCH2OH;HCOOCH2CH3.
本题解析:
本题难度:一般
4、简答题 (6分)在某有机物A的分子中,其结构简式如下图。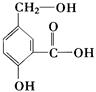
(1)A跟NaOH溶液反应的化学方程式是?
(2)A跟NaHCO3溶液反应的化学方程式是?
(3)A在一定条件下跟Na反应的化学方程式是:?
参考答案:(1) ;
;
(2) + NaHCO3
+ NaHCO3
 + H2O+CO2↑;
+ H2O+CO2↑;
(3) 2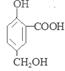 +6Na
+6Na 2
2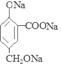 +3H2↑。
+3H2↑。
本题解析:A 中含有羧基与酚羟基,都能与NaOH发生反应,而醇羟基不能发生反应。所以反应的方程式为:
中含有羧基与酚羟基,都能与NaOH发生反应,而醇羟基不能发生反应。所以反应的方程式为: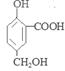 +2NaOH
+2NaOH
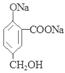 +2H2O。(2)A中只有羧基能与NaHCO3溶液反应。该反应的的化学方程式是
+2H2O。(2)A中只有羧基能与NaHCO3溶液反应。该反应的的化学方程式是 + NaHCO3
+ NaHCO3
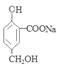 + H2O+CO2↑;(3)无论是醇羟基、酚羟基还是羧基都能与金属Na发生反应。因此A在一定条件下跟Na反应的化学方程式是2
+ H2O+CO2↑;(3)无论是醇羟基、酚羟基还是羧基都能与金属Na发生反应。因此A在一定条件下跟Na反应的化学方程式是2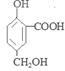 +6Na
+6Na 2
2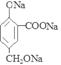 +3H2↑。
+3H2↑。
本题难度:一般
5、填空题 在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为

已知:
①化合物A,其分子式为C9H10O,它既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与金属钠或NaOH溶液反应生成B;
②B发生臭氧化还原水解反应生成C,C能发生银镜反应;
③C催化加氢生成D,D在浓硫酸存在下加热生成E;
④E既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与NaOH溶液反应生成F;
⑤F发生臭氧化还原水解反应生成G,G能发生银镜反应,遇酸转化为H(C7H6O2)。
请根据上述信息,完成下列填空:
(1)写出下列化合物的结构简式(如有多组化合物符合题意,只要写出其中的一组)
A______________,C_____________,E________________.
(2)写出分子式为C7H6O2的含有苯环的所有同分异构体的结构简式:
______________________________________
参考答案:(1)A: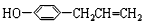 ;B:
;B: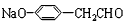 ;C:
;C: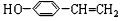
(2)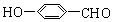 、
、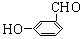 、
、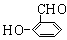 、
、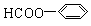 、
、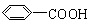
本题解析:
本题难度:一般