| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《原电池原理》试题特训(2017年最新版)(六)
参考答案:B 本题解析:A、锂离子电池可以充电再次使用,属于二次电池,正确;B、铜锌原电池中铜为正极,故电流由铜流向锌,而电子是由锌流向铜,错误;C、Zn失去电子生成Zn2+发生氧化反应,正确,D.锌锰干电池中,锌电极是负极,正确。 本题难度:一般 2、简答题 (10分)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: |
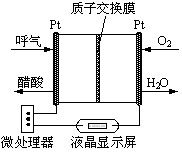
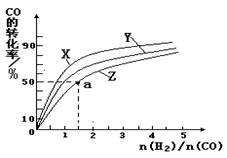
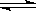 ?CH3OH(g) 的平衡常数K =?。
?CH3OH(g) 的平衡常数K =?。参考答案:(1)CD?(2)CH3CH2OH+H2O-4e-=CH3COOH+4H+?
(3)CH3OH(g)+3/2O2(g) =CO2(g)+ 2H2O(g)?△H=-651kJ・mol-1?
(4)①270℃?②4
本题解析:(1)增大浓度、升高温度、增大压强和使用催化剂都能加快化学反应速率,否则,化学反应速率会降低,故选CD。(2)原电池中的负极失去电子,又因是酸性的燃料电池,所以负极反应式为:CH3CH2OH+H2O-4e-=CH3COOH+4H+。(3)将(3)中第2个热化学方程式*2在和(3)中的第一个热化学方程式叠加再减去题中的热化学方程式即可得解为:CH3OH(g)+3/2O2(g) =CO2(g)+ 2H2O(g)?△H=-651kJ・mol-1。
点评:本题考查学生有关化学平衡以及热化学知识,学生可以根据所学知识来回答,难度较大。
本题难度:困难
3、填空题 (6分) 由A、B、C、D四种金属按下表中装置进行实验,根据实验现象回答①②③
参考答案:(6分)?2H+ +2e--==?H2↑;C→B;D>A>B>C
本题解析:金属A不断溶解,说明A是负极,失去电子,发生氧化反应,则A的金属性强于B的。其中正极是氢离子放电生成氢气,电极反应式是2H+ +2e--==?H2↑;C的质量增加,这说明C是正极,溶液中的铜离子放电,生成铜而形成,则电流方向是C→B,其中B的金属性强于C的;A和D构成原电池时,A上有气体产生,说明A是正极,溶液中的氢离子放电生成氢气,所以D的金属性强于A的。综上所述,四种金属的金属性强弱顺序是D>A>B>C。
点评:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应,据此可以进行有关的判断。
本题难度:一般
4、选择题 下列叙述正确的是( )
A.在原电池的正极和电解池的阳极上发生的都是氧化反应
B.实验室用惰性电极电解NaCl溶液,阴、阳两极收集到的气体体积之比为2:1
C.用铜作电极电解稀硫酸,可能发生反应:Cu+H2SO4
? |
参考答案:A、原电池正极上得电子发生还原反应,故A错误;
B、用惰性电极电解NaCl溶液的电解方程式为2NaCl+2H2O?电解?.?2NaOH+H2↑+Cl2↑,根据方程式知,氢气和氯气的体积之比为1:1,故B错误;
C、用铜作电极电解稀硫酸,刚开始时,阳极上铜失电子,阴极上氢离子得电子,所以可能发生反应:Cu+H2SO4?电解?.?CuSO4+H2↑,故C正确;
D、用惰性电极电解稀硫酸的过程中,阳极上析出氧气,阴极上析出氢气,实则电解水,溶液的溶质不变,溶剂的量减少,导致溶液中氢离子浓度增大,pH减小,故D错误.
故选C.
本题解析:
本题难度:一般
5、计算题 由Zn―Cu―H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:
(1)原电池的_______极生成氢气_______L(标准状况)。
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到_________kJ的热量。
(3)若将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为_____________。
参考答案:
(1)正,2.24L(2)28.58(3)12.9g
本题解析:略
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《化学实验的.. | |