1、填空题 (1)下列装置属于原电池的是_____________;

(2)在选出的原电池中,______ 是负极,发生_____________ 反应 ,______是正极,该极的现象___________________________;
(3)此原电池反应的化学方程式为___________________________。
参考答案:(1)⑤
(2)Fe;氧化;Cu;有气体产生
(3)Fe+H2SO4==FeSO4+H2↑
本题解析:
本题难度:一般
2、选择题 下列说法违背化学原理的是
A.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
B.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量较高
C.A(g)+3B(g)  2C(g)达平衡后,恒温,增压,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,恒温,增压,平衡正向移动,平衡常数K值增大
D.在KI溶液中加入氯化银固体,沉淀变成黄色,说明同温度下Ksp(AgI)< Ksp(AgCl)
参考答案:C
本题解析:C项:平衡常数K值减小,故错。故选C。
点评:本题重点考查的是化学基本原理的相关知识。难度易。比较基础,注意基础知识的积累和掌握。
本题难度:一般
3、填空题 在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如下图所示。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。
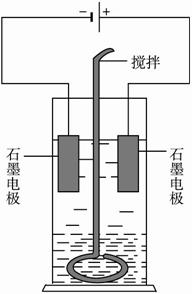
根据上述实验完成:
(1)阳极上的电极反应式为________________。
(2)阴极上的电极反应式为________________。
(3)原上层液体是________。
(4)原下层液体是________。
(5)搅拌后两层液体颜色发生变化的原因是________________。
(6)要检验上层液体中含有的金属离子,其方法是________,现象是________________。
参考答案:(1)2I--2e-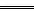 I2
I2
(2)2H++2e-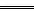 H2↑
H2↑
(3)KI(或NaI等)水溶液
(4)CCl4(或CHCl3等)
(5)I2在CCl4中的溶解度大于在水中的溶解度,所以绝大部分I2都转移到CCl4中
(6)焰色反应 透过蓝色钴玻璃观察火焰呈紫色(其他合理答案也可。例如,若③中答NaI水溶液,这里答火焰呈黄色)
本题解析:(1)使用惰性电极(石墨)电解溶液时,阳极上离子按照I-、Br-、Cl-、OH-顺序失电子,结合题目给出的“下层液体呈紫红色”,可知这里是I-失电子生成I2。所以阳极反应是:2I--2e-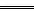 I2。
I2。
(2)电解时,阴极发生得电子反应,溶液中能得电子变成气体的只有H+,生成H2。所以负极反应是:2H++2e- H2↑。
H2↑。
(3)两种无色的互不相溶的中性液体,一为水溶液,一为有机溶剂。根据对电解过程的分析,反应会产生I2,最后I2会被有机溶剂萃取。因为最后下层液体呈紫红色,所以有机溶剂密度比水大。上层的水溶液应该为含I-的盐溶液,例如KI溶液、NaI溶液等。下层液体为CCl4、CHCl3等密度比水大的有机溶剂。
(4)见(3)的分析。
(5)I2在有机溶剂中的溶解度大于在水中的溶解度,所以绝大部分I2都转移到有机溶剂中,有机溶剂显示出紫红色。
(6)可以通过焰色反应来检验。若前面填KI,则这里正确的方法是:用铂丝蘸取少量溶液放在无色火焰上灼烧,透过蓝色钴玻璃可观察火焰呈紫色(其他合理答案也可。例如,若③中答NaI水溶液,这里答火焰呈黄色)。
本题难度:一般
4、简答题 对图中两极进行必要的连接并填空:
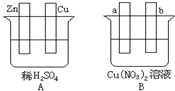
(1)在图A中,使铜片上冒H2气泡.则加以必要的连接后的装置叫______;两极发生的电极反应式为:锌板、______;铜板、______.
(2)在图B中,a、b为惰性电极,进行必要的连接后使a极析出铜,则b极出现的现象是______;该装置叫______;该反应总的化学方程为______.
(3)如将图A中Zn、Cu两极与图B中a、b作必要的连接后,也能产生与(1)、(2)完全相同的现象,则Zn极连______极,Cu极连______极(填a或b).经过一段时间后,停止反应并搅匀溶液,图B中溶液的pH______(填写“升高”、“降低”或“不变”),欲使溶液恢复至与反应前完全一致,则应加入的一定量的物质是______
A.CuOB.Cu(OH)2C.Cu2(OH)2CO3D.CuSO4.
参考答案:(1)在A图中,使铜片上冒H2气泡,则铜片作正极,锌作负极,该电池属于原电池,锌电极上失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+,电极上氢离子得电子发生还原反应,电极反应式为:2H++2e-=H2↑,
故答案为:原电池;Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)在B图中(a,b都为惰性电极),使a极析出铜,电极材料不能得失电子,所以该装置是电解池,a是阴极,阴极上铜离子得电子发生还原反应,电极反应式为:Cu+2e-=Cu 2+,b是阳极,阳极上氢氧根离子放电生成氧气,所以b电极上有气体生成,电池反应式为:2Cu(NO3)2+2H2O电解.2Cu+O2↑+4HNO3,
故答案为:有气体生成;电解池;2Cu(NO3)2+2H2O电解.2Cu+O2↑+4HNO3;
(3)如将图A中Zn、Cu两极与图B中a、b作必要的连接后,也能产生与(1)、(2)完全相同的现象,a作阴极,b作阳极,阳极连接原电池正极,阴极连接原电池负极,所以锌连接a,铜连接b;
B中阳极上氢氧根离子放电生成氧气,阴极上铜离子放电生成铜,导致溶液中氢离子浓度增大,溶液的pH降低,根据“析出什么加入什么”的原则知,B中析出的物质相当于氧化铜,要使溶液恢复原状,应该加入氧化铜,故选A,
故答案为:a;b;降低;A.
本题解析:
本题难度:一般
5、选择题 能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是?
[? ? ]
A.用铜片作阴、阳电极,电解氯化铜溶液
B.用铜片作阴、阳电极,电解硫酸钾溶液
C.铜锌合金在潮湿空气中发生电化学腐蚀
D.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液
参考答案:B
本题解析:
本题难度:一般