1、选择题 下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
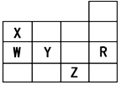
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
参考答案:D
本题解析:根据元素在周期表中的位置关系可知:X是N;W是P;Y是S;R是Ar;Z是Br. A.常压下五种元素的单质中Br2单质是液态,而S、白磷、红磷为固态。所以Br2单质的沸点不能可能最高。错误。B、S2-离子的核外有18个电子,与Ar原子的相同;而Br-离子的核外有36个电子,电子层结构Kr相同。错误。C、P的氢化物PH3的分子间以分子间作用力结合,而NH3的分子间除了存在分子间作用力外,还存在氢键,增加了分子之间的相互作用。所以沸点不如NH3沸点高。错误。D、S元素的原子半径比P小,原子失去电子难,获得电子容易,所以S的非金属性比P元素的非金属性强。正确。
本题难度:一般
2、选择题 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知:
?
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
参考答案:A
本题解析:A、W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知W为N元素,则X、Y、Z分别为O、S、Cl,则三者的非金属性由强到弱的顺序为:O>Cl>S,所以它们的氢化物稳定性最弱的是H2S,正确; C、单核阴离子还原性O2-<S2-,错误;D、Cl2的中的氯元素的化合价为0,是中间价态,既能升高,又能降低,错误。
本题难度:一般
3、选择题 下列对一些实验事实的理论解释正确的是?
选项
| 实?验?事?实
| 理?论?解?释
|
A.
| NH3溶于水形成的溶液微弱导电
| NH3是弱电解质
|
B.
| 氮气与氧气反应条件苛刻
| 氮元素的非金属性不强
|
C.
| 1体积水可以溶解600体积氯化氢气体
| 氯化氢分子很稳定
|
D.
| HF的沸点高于HCl
| HF分子间存在氢键
参考答案:D
本题解析:氨气溶于水形成的溶液导电,一水合氨是电解质,氨气是非电解质,A不正确;氮气中含有三键,键能大,氮气稳定性强,但氮元素是活泼的非金属元素,B不正确;氯化氢的溶解性和氯化氢分子的稳定性没有关系,C不正确;HF的沸点高于HCl,这是由于HF分子间存在氢键,D正确,答案选D。
点评:该题是中等难度的试题,试题基础性强侧重对基础知识的巩固和训练。试题紧扣教材,也有了调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和抽象思维能力。
本题难度:一般
4、选择题 下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是原周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。
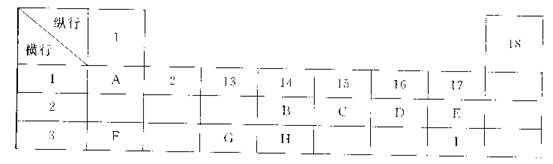
(1)B、C两元素中非金属性较强的是?(写出元素名称),请设计一个简单的实验证明这一结论?。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
?
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式:?。
?(4)I元素在周期表里的位置在第?周期、第?族。?实验室中采用右图所示装置模拟工业上同时制取元素A和I
的单质过程:
①写出电极C1上发生反应的电极反应式?。
②当电极上产生112mL(标准状况)元素I单质气体时(假设
气体完全逸出,溶液体积不变),烧杯中溶液的pH=?。
(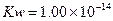 ) )
参考答案:
(13分)
(1)(3分)氮(1分),取碳酸钠或碳酸氢钠溶液置于试管中,向其中滴加稀硝酸,观察是否有无色无味的气体产生,HNO3+NaHCO3===NaNO3+H2O+CO2↑2HNO3+Na2CO3===2NaNO3+H2O+CO2↑(2分)(可不写化学方程式,其他合理的答案也得分)
(2)(2分)Al2O3+2OH-+3H2O===2[Al(OH)4]-(2分)
(3)(2分)2Na2O2+2H2O===4NaOH+O2↑(2分)
(4)(6分)第三周期,VIIA族(2分);
①2Cl-→Cl2↑+2e-(分)
②13(2分)
本题解析:略
本题难度:一般
5、选择题 下列说法中正确的是(?)
A.处于最低能量的原子叫做基态原子
B.在同一能级上运动的电子,其运动状态有可能完全相同
C.电子的运动与行 星相似,围绕原子核在固定的轨道上高速旋转
D.同一原子中,1s、2s、3s电子的能量逐渐增加,2p、3p、4p能级的轨道数依次增多
参考答案:A
本题解析:A 在同一能级上运动的电子,如果自选状态相同,则一定处在不同的轨道(如2Px、2Py、2Pz),如果处在同一轨道,则一定自选状态相反。事实上,没有两个电子的运动状态是完全相同的,B错误。根据量子力学理论可知,C错误。同一原子中,1s、2s、3s电子的能量逐渐增加,但2P、3P、4P能级的轨道数相同,D错误。
点评:本题主要考查原子结构的基本概念,难度不大,只要熟记掌握相关概念即可解决。
本题难度:简单
|