1、选择题 关于电解NaCl水溶液,下列叙述正确的是?
A.将阳极产生的气体通入淀粉KI溶液,溶液变蓝色
B.阴极发生氧化反应,阳极发生还原反应
C.阴极发生还原反应,得到金属钠
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
参考答案:A
本题解析:略
本题难度:一般
2、选择题 下列关于物质的制取的叙述正确的是( )
A.用惰性电解饱和氯化钠溶液时,与电源正极相连的电极上得到是氢气
B.用惰性电解饱和氯化钠溶液时,溶液的碱性增强
C.电解熔融氯化钠时,与电源正极相连的电极上得到是金属钠
D..电解熔融氯化钠时,与电源负极相连的电极上得到是氯气
参考答案:A、电解池中与电源正极相连的电极是阳极,用惰性电解饱和氯化钠溶液时,与电源正极相连的电极上是氯离子发生失去电子的氧化反应,会生成氯气,故A错误;
B、电解饱和氯化钠溶液所获得的产物是氢氧化钠溶液,碱性增强,故B正确;
C、电解池中与电源正极相连的电极是阳极,电解熔融氯化钠时,阳极是氯离子发生失去电子的氧化反应,是生成氯气的过程,故C错误;
D、电解池中与电源负极相连的电极是阴极,电解熔融氯化钠时,阴极上是氢离子发生得电子的还原反应,是生成氢气、氢氧化钠的电极,故D错误.
故选B.
本题解析:
本题难度:简单
3、选择题 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色。下列说法中不正确的是(?)

A.x是正极,y是负极
B.x是负极,y是正极
C.a极和Pt都有气泡产生
D.U形管中溶液的碱性增强
参考答案:A
本题解析:根据装置特点可知属于电解池,b极附近溶液呈蓝色,说明该极有单质碘生成,即I-离子失去电子,被氧化,所以该电极是阳极,则y是电源的正极,x是负极,c是阴极,Cu2+放电析出铜。Pt是阳极,OH-放电生成氧气。a是阴极,H+放电,放出氢气。所以答案是A。
本题难度:一般
4、简答题 (16分) 研究发现铜具有独特的杀菌功能, 能较好地抑制病菌的生长。现有工业上由辉铜矿石(主要成分Cu2S)的冶炼铜两种方案:
Ⅰ 火法炼铜在1200℃发生的主要反应为:
①2Cu2S+3O2=2Cu2O+2SO2 ; ②2Cu2O+Cu2S= 6Cu+SO2↑
此方案的尾气可以用表中方法处理
方法1
| 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫,其部分热化学方程式为:
2CO(g)+SO2(g)= S(g)+2CO2(g) ΔH="+8." 0 kJ・mol-1
2H2(g)+SO2(g)= S(g)+2H2O(g) ΔH="+90." 4 kJ・mol-1
|
方法2
| 用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸

|
Ⅱ“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2)氧化为Fe2(SO4)3,并使溶液酸性增强;利用Fe2(SO4)3作氧化剂溶解辉铜矿石,溶液酸性又进一步增强,过滤未溶解完的辉铜矿石,在滤液中加入足量的铁屑,待反应完全后过滤出铜和剩余的铁屑,得溶液Xml(设整个过程中其它杂质不参与反应,不考虑溶液离子水解)。其流程如图:
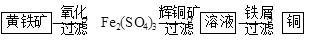
(1)Ⅱ相对于Ⅰ的优点是______________________________。(说一点即可)
(2)Ⅰ中反应2Cu2O+Cu2S= 6Cu+SO2↑氧化剂是________
(3)已知CO的燃烧热283. 0 kJ・mol-1,写出S(g)与O2(g)反应生成SO2(g)的热化学方程式___________。
(4)若用Ⅰ中方法2吸收尾气,则开始时阳极的电极反应式为________________。
(5)写出Ⅱ中黄铁矿氧化过程的化学反应方程式______________________________
(6)假设Ⅱ中每一步都完全反应,消耗掉标况下空气5×22.4VL(氧气体积分数为20%),则所得c(Fe2+)=________________(可以写表达式)。
参考答案:(共16分)
(1)①能大大降低能源消耗;利于减少污染(写一条且正确得2分)
(2)Cu2O、Cu2S(2分,写名称也可得2分,写一个得1分)
(3)S(g)+O2(g)=SO2(g) ΔH=-574.0kJ・mol-1(3分,没有写聚集状态扣1分,没有写负号1分,没有数字和单位扣1分)
(4)HSO3-+H2O-2e-===SO42-+3H+ (左边出现HSO3-得1分,共3分)
(左边出现HSO3-得1分,共3分)
(5)4FeS2+15O2+2H2O 2Fe2(SO4)3+2H2SO4(没有写条件扣1分,没有配平扣1分,共3分)
2Fe2(SO4)3+2H2SO4(没有写条件扣1分,没有配平扣1分,共3分)
(6)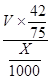 mol/L或
mol/L或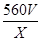 mol/L(3分,有
mol/L(3分,有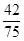 可以得1分)
可以得1分)
本题解析:(1)①方法二消耗了电能,方法一没有消耗电能,所以能大大降低能源消耗;利于减少污染。
(2)2Cu2O+Cu2S=6Cu+SO2↑反应中铜元素的化合价从+1降低到0,所以氧化亚铜和硫化亚铜都做氧化剂。
(3)反应①:2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=+8.0kJ・mol-1,和CO的燃烧热283.0kJ・mol-1,则反应②:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0kJ・mol-1,根据盖斯定律,②×2-①,反应热为-283×2-8=574kJ・mol-1,所以热化学方程式为:S(g)+O2(g)=SO2(g) ΔH=-574.0kJ・mol-1。(4)阳极失去电子化合价升高,从图分析亚硫酸氢根失去电子产生硫酸根离子,电极反应为:HSO3-+H2O-2e-===SO42-+3H+。(5)黄铁矿被氧化成硫酸铁,方程式为:4FeS2+15O2+2H2O 2Fe2(SO4)3+2H2SO4。
2Fe2(SO4)3+2H2SO4。
(6)Cu2S+10Fe3++4H2O=2Cu2++10Fe2++8H++SO42-,Cu2++Fe=Fe2++Cu,2H++Fe=Fe2++H2,根据硫原子守恒,硫元素最后都到硫酸亚铁,所以有关系:15O2----8.4FeSO4,亚铁离子物质的量为8.4V/15,亚铁离子浓度为: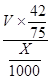 mol/L或560
mol/L或560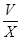 mol/L。
mol/L。
考点:氧化还原反应,盖斯定律,电解原理的应用,原子守恒法计算。
本题难度:困难
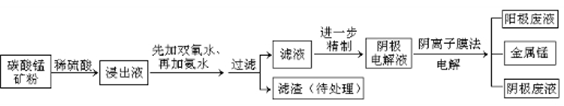
5、填空题 28(15分)某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:
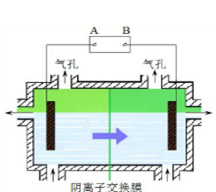
阴离子膜法电解装置如图所示:
(1)写出用稀硫酸溶解碳酸锰反应的离子方程式 。
(2)在浸出液里锰元素只以Mn2+的形式存在,且滤渣中也无MnO2,请解释原因 .
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
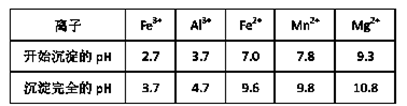
加氨水调节溶液的pH等于6,则滤渣的成分是 ,滤液中含有的阳离子有H+和 。
(4)电解装置中箭头表示溶液中阴离子移动的方向,则A电极是 极。实际生产中,以石墨为电极,阳极区以稀硫酸为电解液,阳极的电极反应式为 。
(5)该工艺之所以采用阴离子交换膜,是为了防止Mn2+进入阳极区发生副反应生成MnO2造成资源浪费,写出该副反应的电极反应式 。
参考答案:(1)MnCO3+2H+=Mn2++CO2↑+H2O
(2)MnO2在酸性条件下被二价铁还原为Mn2+
(3)Al(OH)3、Fe(OH)3;Mn2+、Mg2+、NH4+
(4)负极;4OH--4e-=O2↑+2H2O 或2H2O-4e-=O2↑+4H+
(5)Mn2++2H2O-2e-=MnO2+4H+
本题解析:将碳酸锰矿粉溶于稀硫酸中,MnCO3、FeCO3、MgO、Al2O3都和稀硫酸反应生成硫酸盐,酸性条件下,MnO2被亚铁离子还原生成Mn2+,SiO2以沉淀析出,然后向浸出液中先加双氧水,再加氯水,并调节溶液的pH到6,根据氢氧化物沉淀需要的pH,当pH=6时Fe3+、Al3+完全转化为沉淀,溶液中存在Mn2+、Mg2+、NH4+,则滤渣为Al(OH)3、Fe(OH)3,然后进一步精制,再利用离子交换膜电解。
(1)碳酸锰和稀硫酸反应生成硫酸锰,二氧化碳和水,离子方程式为MnCO3+2H+=Mn2++CO2↑+H2O;(2)加入双氧水时将亚铁离子氧化为铁离子,根据氢氧化物沉淀需要的pH知,pH=6时Fe3+、Al3+完全转化为沉淀,溶液中存在Mn2+、Mg2+、NH4+,则滤渣为Al(OH)3、Fe(OH)3,滤液中含有的阳离子为H+、Mn2+、Mg2+、NH4+;(3)酸性条件下,MnO2被亚铁离子还原,亚铁离子被氧化生成铁离子,所以在浸出液里锰元素只以锰离子的形式存在,且滤渣中无MnO2;(4)根据阴离子移动方向可知,左边电极是阴极,右边电极是阳极,则连接阴极的电极A是电源的负极,阳极上氢氧根离子放电生成氧气,电极反应为4OH--4e-=O2↑+2H2O 或2H2O-4e-=O2↑+4H+;(5)锰离子不稳定,易被氧化生成二氧化锰,所以阳极的副反应为Mn2++2H2O-2e-=MnO2+4H+。
考点:物质分离和提纯的方法和基本操作综合应用、电解原理
点评:本题主要考查混合物的分离和提纯,侧重考查学生对知识的综合运用能力,涉及内容较多,难度较大。
本题难度:困难