1、选择题 下列各物质中所含的少量杂质,用括号内的物质能除去,并且不引进其他杂质的是( )
A.二氧化碳中所含的氯化氢(NaOH溶液)
B.氢气中所含的硫化氢(硫酸铜溶液)
C.乙酸乙酯中所含的乙酸(乙醇)
D.氯化钠溶液中所含的氯化钡(硫酸)
2、选择题 能使干燥的红色布条褪色的是( )
A.液氯
B.新制氯水
C.CaCl2溶液
D.盐酸
3、计算题 实验室迅速制备少量氯气可利用如下所示的反应
2KMnO4?+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O ; 当参加反应的氧化剂的物质的量是1mol时,回答下列问题:
(1)被氧化的还原剂的物质的量是多少?
(2)产生标准状况下的氯气的体积多少升?
4、填空题 (8分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。比Cl2更好。
⑴在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑ +2H2O
+2H2O
用方法二制备的ClO2更适合用于饮用水消毒,其主要原因是?。
⑵用ClO2处理过的饮用水(pH 5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2-)。
饮用水中的ClO2、ClO2-含量可用连续碘量法进行测定。ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如下图所示。当pH≤2 .0时,ClO2-也能被I-完全还原为Cl-。反应生成的I2用标准Na2S2O3溶液滴定;2Na2S2O3+ I2= Na2S4O6 + 2NaI
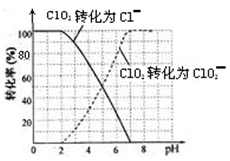
①请写出pH≤2 .0时ClO2--与I-反应的离子方程式?。
②请完成相应的实验 步骤:
步骤:
步骤1:准确量取V mL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用c mol・L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
步骤5:?。
步骤6:再用c mol・L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2?mL。
③根据上述分析数据,测得该饮用水中ClO2-的浓度为? ?mol・L-1(用含字母的代数式表示)。
?mol・L-1(用含字母的代数式表示)。
5、选择题 丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是( )
①新制氯水久置后→浅黄绿色消失 ②淀粉溶液遇碘化钾→蓝色
③蔗糖中加入浓硫酸搅拌→白色④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色.
A.①②④⑤
B.②③④⑤
C.①④⑤
D.①②③④⑤