1��ѡ���� �ò����缫���500mL��KNO3��Cu��NO3��2�Ļ����Һһ��ʱ���������������11.2L��״���µ����壬ԭ��Һ��Cu2+�����ʵ���Ũ��Ϊ��������
A��0.5?mol/L
B��2?mol/L
C��1?mol/L
D����ȷ��
�ο��𰸣�������Һ�����ӷŵ�˳����д�缫��Ӧ����Һ������������������ʧ�������������������ӷŵ�˳��Cu2+��H+�������缫��ӦΪ��4OH--4e-=2H2O+O2���������缫��ӦΪ��Cu2++2e-=Cu 2H++2e-=H2����������������11.2L��״���µ��������ʵ���Ϊ0.5mol�����ݵ����غ�缫��Ҫ����Ϊ4��0.5mol=2mol����������ת�Ƶ���1mol��ͭ���ӵõ�����1mol����Ӧ��ͭ�������ʵ���0.5mol������Cu2+�����ʵ���Ũ��=0.5mol0.5L=1mol/L��
��ѡC��
���������
�����Ѷȣ�һ��
2������� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش�
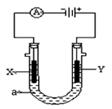
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ?����X�������۲쵽��ʵ��������?��
��Y�缫�ϵĵ缫��ӦʽΪ?������õ缫��Ӧ����ķ�����?��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ�����?���缫��ӦΪ?��
��Y�缫�IJ�����?���缫��ӦʽΪ?��
��˵�������ʷ����ĵ缫��Ӧ����д����
�ο��𰸣���1����2H++2e-��H2��?�ų����壬��Һ���
��2Cl��2e-=Cl2��?��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
��2���ٴ�ͭ? Cu2++2e-=Cu?�ڴ�ͭ Cu��2e-=Cu2+
�����������1����X�缫���Դ�ĸ�������������������Һ�е������ӷŵ磬�缫��Ӧʽ��2H++2e-��H2����������Һ�������ӷŵ磬�ƻ���������Χˮ�ĵ���ƽ�⣬������Һ��OH��Ũ��������Һ������ǿ������X�������۲쵽��ʵ�������Ƿų����壬��Һ��졣
��Y�缫����������Һ�е������ӷŵ磬�缫��Ӧʽ��2Cl��2e-=Cl2������������ǿ�����ԣ��ݴ˿��Խ��м��飬���巽���ǰ�ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
��2����ͭ����ʱ����ͭ�������͵�Դ����������������������Ӧ����ͭ���������͵�Դ�ĸ�����������Һ�е�ͭ���ӷŵ磬������ԭ��Ӧ��
�����������Ǹ߿��ж�����ͺ���Ҫ�Ŀ��㣬���ڻ���������Ŀ��飬�ѶȲ�����Ĺؼ�����ȷ���ԭ�����Լ���Һ�����ӵķŵ�˳������������ѧ����Ӧ�������淶�Ĵ������������ѧ��������û���֪ʶ���ʵ�������������
�����Ѷȣ�һ��
3�������
2010�����˻����ҹ����ݳɹ��ٰ죬�������˻������˻�������
(1)�������˻��桰���������ñ���(C3H8)��ȼ�ϣ�ȼ�պ�IJ���Ϊˮ�Ͷ�����̼����298Kʱ��1mol������ȫȼ������CO2��Һ̬ˮ�ų�2221. 5 kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ__________________��
��֪����298Kʱ��
C3H8(g)=C3H6(g) +H2(g)����H= +124.2 kJ/mol��
H2(g)+O2(g)=H2O(l);?��H= -285.8 kJ/mol��
��l mol C3H8��ȫȼ������CO2��Һ̬ˮʱ�ų���������___________kJ��
(2)������һ�������ĺ������У���ˮ��Դ�dz��ḻ��
�ٺ�����������Ϊ����������Ϊ��������ˮΪ�������Һ�������е�����������Ӧ��������������ܷ�ӦΪ��4Al+3O2+6H2O=4Al(OH)3������˵����ȷ����_________����д�����ĸ����
a����ع���ʱ�����������缫�ص������缫
b�����缫������״�ȿ�״������O2�ŵ�
c����ˮ�е�OH-�����缫�����ƶ�
�������£��ö��Ե缫���200mL l.5 mol/Lʳ��ˮ�� ���2minʱ���������ռ���448 mL���壨��״���£���д���õ�ⷴӦ�����ӷ���ʽ_________________��������ǰ����Һ��������䣬��������Һ��pHΪ_____��
�ο��𰸣�(1)C3H8(g)+5O2(g)=3CO2(g) +4H2O(l); ��H=-2221.5 kJ/mol�� 2059.9
(2)��be����2Cl-+2H2O 2OH-+H2��+Cl2����13
2OH-+H2��+Cl2����13
���������
�����Ѷȣ�һ��
4��ѡ���� ��ʾ���б仯�Ļ�ѧ������ȷ����
A��Na2CO3��ˮ�⣺CO32��+H2O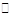 H2CO3+2OH��
H2CO3+2OH��
B����ʯī�缫�������ͭ��Һ��2Cu2+��4OH�� 2Cu��O2����2H2O
2Cu��O2����2H2O
C����������������ʴ��������ӦʽΪ��O2 ��2H2O��4e- = 4OH��
D������ʹ���Ը��������Һ��ɫ��2MnO4��+5C2O42��+16H+=2Mn2++10CO2��+8H2O