|
�߿���ѧ֪ʶ����ɡ�������ʵ���ƽ�⡷������ѵ��2017�����°棩(��)
2017-11-11 03:50:38
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1��ѡ���� ǿ������ʵı��������� �� ��
A����������
B����Է�������
C������̶�
D���ܽ��
|
�ο��𰸣�C
�������������ʵĵ�����ֻ����Һ������Ũ���йء�������Ũ��Խ������Խ��ǿ�����ָ����Һ����ȫ���롣�������ָ����Һ�в��ֵ��롣����ǿ����ʲ��ǵ����������������ǿ��Ҳ�����ж�ǿ������ʵ�����˭ǿ˭����
���ʲ������ˮ��Һ������״̬������ȫ����Ļ��������ǿ����ʲ��ֵ�������������
��ѡC
�����Ѷȣ�һ��
2��ѡ���� �����ͬ����ҺPHҲ��ͬ������ʹ�����Һ��������������Һǡ���к�ʱ�����������������Ƶ����ʵ�����������
A����ͬ
B���кʹ���Ķ�
C���к�����Ķ�
D������ȷ��
�ο��𰸣��Ȼ�����ǿ����ʣ�������������ʣ���ˮ��Һ����ڵ���ƽ�⣬����pH��ȵ�����ʹ��ᣬ�����Ũ��С�ڴ��ᣬ�������pH�������ᣬ��������ʵ����������ᣬ��������ᶼ��һԪ�ᣬ������ʵ���Խ���к�ʱ��Ҫ����������Խ�࣬���Դ������ĵ��������ƶ࣬
��ѡ��B��
���������
�����Ѷȣ���
3��ѡ���� ����ʵ������в������������Ӧ��ͼ����ȷ���ǣ�������
A��NaAlO2��Һ�м�������
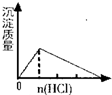
B��SO2����ͨ����ˮ��

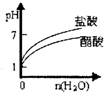
C��pH=2�Ĵ�����������Һ�ֱ��ˮϡ��
D������ͨ�������Һ��
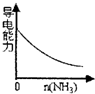
�ο��𰸣�A����NaAlO2��Һ�м������ᣬ������Ӧ�ֱ�ΪAlO2-+H++H2O�TAl��OH��3����Al��OH��3��+3H+�TAl3++3H2O����Ӧ��ʼʱ�г������ɣ�Ȼ������ܽ⣬��A��ȷ��
B��SO2����ͨ����ˮ�У�������ӦBr2+SO2+2H2O�TH2SO4+2HBr����Ӧ����Һ������ǿ��pH��С������ˮ��Һ�����ԣ���ʼʱpH��7����B����
C������Ϊ���ᣬ��ˮϡ��ʱ��һ�����룬pH�仯������С����������ôϡ�ͣ���Һ�������ԣ������ܳʼ��ԣ���C����
D������ͨ�������Һ�У���Ӧ����ǿ����ʴ���泥���Һ����������ǿ����D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� ��1mol/L���������ʵ���Һ�У�ˮ�ĵ���̶������ǣ�������
A��Na2CO3
B��NaHCO3
C��NaCl
D��NaHSO4
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� �ش���������:
(1)��һ����Һ��H+��OH-�⣬����Na+��SO42-��Cl-������������ӵ�Ũ�ȷֱ���0.01 mol��L-1��0.0035 mol��L-1��0.004 mol��L-1������Һ��pHΪ??��
(2)Һ��������ˮ�ĵ��룬��д��Һ���ĵ��뷽��ʽ?��
��3���������ӷ���ʽ��д��ȷ����?��?
A��ʯ������Na2CO3��Һ��ϣ�Ca2++CO32��=====CaCO3��?
B��NH4HSO3��Һ��������NaOH��Һ��ϼ��ȣ�
NH4+ + HSO3- +2OH-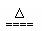 NH3��+SO32-? +2H2O? NH3��+SO32-? +2H2O?
C������������KIO3��Һ��KI��Һ��Ӧ����I2�� IO32-? +5I-+3H2O====3I2+6OH-
D��AgNO3��Һ�м��������ˮ��Ag++NH3��H2O=====AgOH��+NH4+?
E��H2SO4��Ba(OH)2��Һ��Ӧ��Ba2++OH-+H++SO42-="====" BaSO4��+H2O?
F��CuSO4��Һ����H2S���壺Cu2++H2S======CuS��+2H+?
G��AlCl3��Һ�м��������Ũ��ˮ��Al3++4NH3��H2O ="====" AlO2-? +4NH 4+ +2H2O
H�����������Ũ�ȵ�Ba(OH)2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�
Ba2++2OH-+NH4+? +HCO3-="==?" BaCO3��+NH3��H2O+H2O
I��LiAlH4��������ˮ��õ���ɫ��Һ����ѧ����ʽ�ɱ�ʾΪ��
LiAlH4+2H2O ="==LiAlO2" +4H2��
��4�� Na2O2��HCl��Al2O3����������ˮ����ȫ��Ӧ����Һ��ֻ����Na+��H+��Cl-��OH-������Һ�����ԣ���Na2O2��HCl��Al2O3�����ʵ���֮�ȿ���Ϊ?��? Na2O2��HCl��Al2O3����������ˮ����ȫ��Ӧ����Һ��ֻ����Na+��H+��Cl-��OH-������Һ�����ԣ���Na2O2��HCl��Al2O3�����ʵ���֮�ȿ���Ϊ?��?
A.3��2��1? B.2��4��1?C.2��3��1? D.4��2��1
�ο��𰸣�(1) 3
(2) H2O + NH4+  ?NH3��H2O + H+? ?NH3��H2O + H+?
(3) B��H��I��F?
(4)B
�����������
�����Ѷȣ�һ��
|