1、选择题 下列分离或提纯物质的操作方法正确的是
[? ]
①除去KNO3晶体中混有少量的NaCl晶体:冷却结晶
②除去NaCl晶体中混有少量的KNO3晶体:蒸发结晶
③分离含碘的苯溶液:蒸馏
A.仅有②
B.仅有①③
C.仅有②③
D.①②③
2、选择题 可用如图装置制 取(必要时可加热)、净化、收集的气体是
取(必要时可加热)、净化、收集的气体是
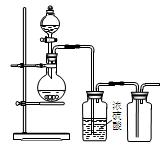
A 、铜和稀硝酸制一氧化氮 B、氯化钠与浓硫酸制氯化氢
、铜和稀硝酸制一氧化氮 B、氯化钠与浓硫酸制氯化氢
C、大理石和稀硫酸制二氧化碳 D、锌颗粒与稀硫酸制氢气
3、填空题 除去Na2CO3粉末中混有的NaHCO3杂质用______方法;用______检验酒精中是否含有水.
4、填空题 电子级钴的氧化物用于半导体工业和电子陶瓷等领域,是一种纯度很高的氧化物。其工业制取流程如下:

(1)实验室过滤所需的仪器有铁架台、铁圈、烧杯、??和漏斗。
(2)滤渣A的成分除过量的Co3(PO4)3和Fe(OH)3外还有?(填化学式),加入CO3(PO4)2的目的是?。
(3)Co与稀硝酸反应生成 Co2+的离子方程式为:?。
(4)滤渣B经过反复洗涤、干燥后,进行灼烧,其热重分析图如下:写出下列化学反应方程式:
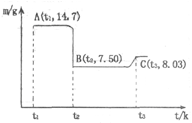
①AB段:?;
②BC段?。
5、填空题 (14分)铬铁矿的主要成分可表示为FeO・Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO?Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③Cr2CO72-+H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有?(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用? ______________?(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是? _______________________ 。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、?、过滤、?、干燥。
(4)下表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr2O7 + 2KCl=K2Cr2O7 ↓+ 2NaCl,该反应在溶液中能发生的理由是_____________________________。
物质
| KCl
| NaCl
| K2Cr2O7
| Na2Cr2O7
|
溶解度(g/100g水)
| 0℃
| 28
| 35.7
| 4.7
| 163
|
40℃
| 40.1
| 36.4
| 26.3
| 215
|
80℃
| 51.3
| 38
| 73
| 376
|
?
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量? ____?(填写试剂)、溶解、过滤、再?(填写试剂)、……灼烧、冷却、称量,得干燥固体m g。计算祥品中氢氧化铝的质量分数为?(用含m、n的代数式表示)。