1、选择题 下列分离或提纯物质的操作方法正确的是
[? ]
①除去KNO3晶体中混有少量的NaCl晶体:冷却结晶
②除去NaCl晶体中混有少量的KNO3晶体:蒸发结晶
③分离含碘的苯溶液:蒸馏
A.仅有②
B.仅有①③
C.仅有②③
D.①②③
参考答案:D
本题解析:
本题难度:一般
2、选择题 可用如图装置制 取(必要时可加热)、净化、收集的气体是
取(必要时可加热)、净化、收集的气体是
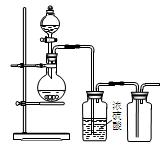
A 、铜和稀硝酸制一氧化氮 B、氯化钠与浓硫酸制氯化氢
、铜和稀硝酸制一氧化氮 B、氯化钠与浓硫酸制氯化氢
C、大理石和稀硫酸制二氧化碳 D、锌颗粒与稀硫酸制氢气
参考答案:B
本题解析:略
本题难度:一般
3、填空题 除去Na2CO3粉末中混有的NaHCO3杂质用______方法;用______检验酒精中是否含有水.
参考答案:NaHCO3不稳定,加热易分解,除去Na2CO3粉末中混有的NaHCO3杂质用加热的方法,加热时发生
2NaHCO3?加热?.?Na2CO3+CO2↑+H2O,检验是否有水生成,可用无水硫酸铜或CuSO4,生成CuSO4?5H2O蓝色晶体.
故答案为:加热;无水硫酸铜(或CuSO4).
本题解析:
本题难度:一般
4、填空题 电子级钴的氧化物用于半导体工业和电子陶瓷等领域,是一种纯度很高的氧化物。其工业制取流程如下:

(1)实验室过滤所需的仪器有铁架台、铁圈、烧杯、??和漏斗。
(2)滤渣A的成分除过量的Co3(PO4)3和Fe(OH)3外还有?(填化学式),加入CO3(PO4)2的目的是?。
(3)Co与稀硝酸反应生成 Co2+的离子方程式为:?。
(4)滤渣B经过反复洗涤、干燥后,进行灼烧,其热重分析图如下:写出下列化学反应方程式:
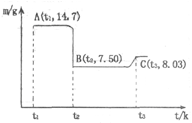
①AB段:?;
②BC段?。
参考答案:(1)玻璃棒(2)Si?调节pH,保证Co2+不沉淀,而使铁离子全部沉淀
(3)3Co+8H++2NO3-=3Co2++4H2O+2NO↑?
(4)CoC2O4 CoO+CO↑+CO2↑? 6CoO+O2
CoO+CO↑+CO2↑? 6CoO+O2 2Co3O4
2Co3O4
本题解析:(1)实验室过滤所需的仪器有铁架台、铁圈、烧杯、玻璃棒和漏斗。(2)在加入硝酸酸化时钴、Fe都与硝酸发生反应得到硝酸钴、硝酸铁而Si不能与稀硝酸发生反应,所以过滤后存在于滤渣A中。因此滤渣A的主要成分除过量的Co3(PO4)3和Fe(OH)3外还有Si。加入CO3(PO4)2的目的是调节pH,保证Co2+不沉淀,而使铁离子全部沉淀。(3)Co与稀硝酸反应生成 Co2+,根据质量守恒定律和电子守恒、电荷守恒,可知该反应的离子方程式为3Co+8H++2NO3-=3Co2++4H2O+2NO↑。(4)滤渣B(CoC2O4)灼烧发生分解反应:CoC2O4 =CoO+CO↑+CO2↑。得到固体为CoO。n(CoC2O4)=14.7g÷147g/mol=0.1mol;根据元素守恒可得m(CoO)=0.1mol×75g/mol=7.5g;而在t3时固体的质量为8.03g.根据质量守恒定律可知在BC段发生了反应:6CoO+O2
=CoO+CO↑+CO2↑。得到固体为CoO。n(CoC2O4)=14.7g÷147g/mol=0.1mol;根据元素守恒可得m(CoO)=0.1mol×75g/mol=7.5g;而在t3时固体的质量为8.03g.根据质量守恒定律可知在BC段发生了反应:6CoO+O2 2Co3O4。
2Co3O4。
本题难度:一般
5、填空题 (14分)铬铁矿的主要成分可表示为FeO・Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO?Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
③Cr2CO72-+H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有?(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用? ______________?(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是? _______________________ 。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、?、过滤、?、干燥。
(4)下表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr2O7 + 2KCl=K2Cr2O7 ↓+ 2NaCl,该反应在溶液中能发生的理由是_____________________________。
物质
| KCl
| NaCl
| K2Cr2O7
| Na2Cr2O7
|
溶解度(g/100g水)
| 0℃
| 28
| 35.7
| 4.7
| 163
|
40℃
| 40.1
| 36.4
| 26.3
| 215
|
80℃
| 51.3
| 38
| 73
| 376
|
?
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量? ____?(填写试剂)、溶解、过滤、再?(填写试剂)、……灼烧、冷却、称量,得干燥固体m g。计算祥品中氢氧化铝的质量分数为?(用含m、n的代数式表示)。
参考答案:(13分)(1)Fe2O3、MgO(2分)PH计或pH试纸(1分)(2)使CrO42-转化为Cr2O72-(1分)
(3)冷却结晶、洗涤(各1分)
(4)K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小)(2分)
(5)NaOH溶液、通入过量二氧化碳。(各1分,合理答案也给分);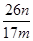 ?(3分)
?(3分)
本题解析:(1)铬铁矿的主要成分可表示为FeO?Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,加入氧气和碳酸钠,发生反应为:①4FeO?Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2↑、②Na2CO3+Al2O3
8Na2CrO4+2Fe2O3+8CO2↑、②Na2CO3+Al2O3 2NaAlO2+CO2↑、③Cr2CO72-+H2O
2NaAlO2+CO2↑、③Cr2CO72-+H2O 2CrO42-+2H+,操作Ⅰ是过滤得到固体X为Fe2O3、MgO;要检测酸化操作中溶液的pH是否等于4.5,普通pH试纸只能测定溶液pH到整数,是近似测定,准确测定需要用pH计或精确pH试纸;
2CrO42-+2H+,操作Ⅰ是过滤得到固体X为Fe2O3、MgO;要检测酸化操作中溶液的pH是否等于4.5,普通pH试纸只能测定溶液pH到整数,是近似测定,准确测定需要用pH计或精确pH试纸;
(2)酸化步骤用醋酸调节溶液pH<5,依据流程图中物质的转化和制备目的可知,结合反应平衡Cr2O72-+H2O 2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72--;
2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72--;
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩,冷却结晶、过滤、洗涤、干燥得到晶体;
(4)依据图表物质的溶解度分析对比,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,这说明K2Cr2O7的溶解度比Na2Cr2O7小(或四种物质中K2Cr2O7的溶解度最小);
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是先利用氢氧化铝的两性,用氢氧化钠溶液溶解氢氧化铝过滤得到滤液中通入二氧化碳生成氢氧化铝沉淀,灼烧干燥得到氧化铝干燥固体m g,依据铝元素守恒计算,样品中氢氧化铝的质量分数= ×100%=
×100%=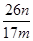 。
。
本题难度:困难