1、选择题 a、b、c、d是短周期元素,在周期表中的相对位置如图所示.c元素原子核外M层电子数是K层电子数的2倍.下列说法中,错误的是( )
A.原子半径:c<b
B.气态氢化物的稳定性:b>d
C.高温下,a单质可与c的氧化物发生置换反应
D.b的最高价氧化物对应的水化物中既含共价键又含离子键
参考答案:a、b、c、d是短周期元素,由在周期表中的相对位置可知,a、b处于第二正确,c、d处于第三周期,a、c处于同主族,b、d处于同族.c元素原子核外M层电子数是K层电子数的2倍,则c元素原子最外层电子数为4,故c为硅元素;a为碳元素,两族元素相邻,所以b为氮元素,d为磷元素.
A、同周期随原子序数增大,原子半径减小,所以原子半径c>d,同主族自上而下,原子半径增大,所以原子半径d>b,所以原子半径c>b,故A错误;
B、同主族自上而下,非金属性加热,所以非金属性d<b,非金属性越强,氢化物越稳定,所以气态氢化物的稳定性:b>d,故B正确;
C、高温下,碳可以与二氧化硅反应置换出硅,硅C正确;
D、b为氮元素,其最高价氧化物对应的水化物为硝酸,属于共价化合物,含有共价键,不含离子键,故D错误.
故选AD.
本题解析:
本题难度:一般
2、选择题 食盐、蔗糖、醋酸、纯碱、汽油、“84消毒液”等是日常生活中经常使用的物质,下列有关说法或表示正确的是( )
A.食盐中阴离子的核外电子排布式为:

B.蔗糖与醋酸的最简式相同
C.纯碱与汽油去除油污的原理相同
D.“84消毒液”中有效成分NaClO的电子式为:
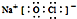
参考答案:A.食盐为氯化钠,它的阴离子为氯离子,Cl-核外电子数为18,核外电子排布式为
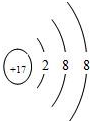
,故A错误;
B.蔗糖的分子式为C12H22O11,最简式为C12H22O11,醋酸的分子式C2H4O2,最简式为CH2O,两者的最简式不同,故B错误;
C.纯碱去油污的原理是纯碱水解溶液呈碱性,油污在碱性条件下水解,生成易溶于水的高级脂肪酸钠和甘油,从而去污,汽油为有机物,油污也为有机物,根据结构相似相溶的原理,汽油能去油污,所以纯碱与汽油去除油污的原理不相同,故C错误;
D.“84消毒液”中有效成分NaClO,它是有钠离子和次氯酸根离子构成,电子式为
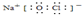
,故D正确.
故选D.
本题解析:
本题难度:一般
3、选择题 下列现象或事实能说明分子之间有间隔的是。
A.用手捏气球,可以使气球变瘪。
B.墙内开花墙外香。
C.100ml的水与100ml的酒精混合,所得溶液的体积小于200ml 。
D.将稀盐酸倒在大理石可以观察到气泡。
参考答案:C
本题解析:根据分子的性质回答,分子间都有间隔,气体的分子间隔大,液体和固体的分子间隔比较小。
A、手捏气球,可以使气球变瘪,不能说明分子,因为气球的体积没有变小。
B、墙内开花墙外香是因为分子运动,和分子间隔无关。
C、100ml的水与100ml的酒精混合,所得溶液的体积小于200ml,能说明分子间有间隔,酒精分子和水分子进入彼此的间隔中,故混合后体积变小。
D、稀盐酸倒在大理石可以观察到气泡是因为发生了化学反应,和分子间隔无关。故选C
本题难度:简单
4、选择题 下列说法不正确的是
[? ]
A.二氧化硫是形成酸雨的一种有毒的酸性氧化物?
B.浓盐酸可以用铝制容器盛装
C.浓硝酸保存需要用棕色瓶?
D.NaClO中既有离子键又有共价键
参考答案:B
本题解析:
本题难度:简单
5、填空题 (10分)有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化 物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。

(1)E元素原子基态时的外围电子排布式为?。
(2)A2F分子中F原子的杂化类型是?,F的气态氧化物FO3分子的键角为?。
(3)CA3极易溶于水,其原因是?,试判断CA3溶于水后,形成CA3・H2O的最合理结构为?(选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为?;

该离子化合物晶体的密度为ρ(g・cm-3)。,则晶胞的体积是?(只要求列出算式)。
参考答案:(1)3d104s1;(2)sp3;120°;
(3)与水分子间形成氢键、两者都是极性分子、与水反应(1分,答到一点就可);b;
(4)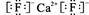 (2分);
(2分);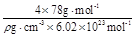 (3分,没带单位不扣分);
(3分,没带单位不扣分);
本题解析:略
本题难度:一般