| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《键参数――键能、键长与键角》高频考点巩固(2017年模拟版)(四)
参考答案:(1)4S24P5 本题解析:(1)非金属性越强,电负性越大,属于电负性最小的是Br,其价电子的排布式是4S24P5。 本题难度:一般 2、填空题 (13分)下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)写出元素g的基态原子核外电子排布式___________________________, h2+中未成对电子数为?。 (2)在b2a2分子中,元素b为?杂化,该分子是?分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为?。 (3) bd2与bf2比较,沸点较高的是_______(填分子式),原因是?。 (4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是?。 A.h位于元素周期表中第四周期第VIII族,属于d区元素 B.e的基态原子中,3p能级为半充满,属于p区元素 C.最外层电子排布式为4s2,一定属于IIA族 D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族 (5)科学研究表明,元素b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为?,其熔点比金刚石?(填“高”或“低”)。 参考答案:(1)1s22s22p63s23p63d54s1(2分)? 4(1分) 本题解析:(1)根据元素在周期表中的位置可知,g是铬元素,原子序数为24,由于半充满或全充满稳定性强,所以根据构造原理可知,基态原子核外电子排布式1s22s22p63s23p63d54s1。H是铁元素,亚铁离子中含有的未成对电子数为4。 本题难度:一般 3、选择题 下列物质只含共价键,不含离子键的是( ? ) 参考答案:B 本题解析: 本题难度:简单 4、选择题 有X、Y、Z三种短周期主族元素,它们在周期表中的位置关系如图,下列有关说法中一定正确的是( ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
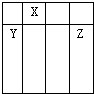
参考答案:由元素在周期表中的相对位置可知X为N元素,Y为Si元素,Z为Cl元素,则
A.X在第二周期,原子半径最小,Y、Z在第三周期,同周期元素从左到右原子半径逐渐减小,则应有Y>Z>X,故A正确;
B.若Y为Si元素,Z为Cl元素,二者形成的化合物为共价化合物,故B错误;
C.若Y为金属元素,若为Mg、Al等,X为非金属元素,故C错误;
D.若Z的最高价氧化物对应的水化物是强酸,则Y元素的最高价氧化物可为非金属氧化物,故D错误.
故选A.
本题解析:
本题难度:简单
5、选择题 含有非极性键的化合物是
[? ]
A.H2O2
B.HCl
C.Cl2
D.NaOH
参考答案:A
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《与量有关的离子方.. | |