1��ѡ���� A��B����Ԫ�ص�ԭ�ӣ������Ƕ����2�������γ��ȶ��ṹ��������ʱ��A�ų�����������B���ɴ˿�֪��
A.�ȶ��ԣ�H2A>H2B
B.��ԭ�ԣ�A2->B2-
C.ԭ�Ӱ뾶��A>B
D.�ǽ����ԣ�A
2��ѡ���� �������ʵ�ת���ڸ��������²���ʵ�ֵ���
A��
B��
C��
D��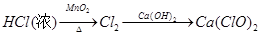
3��ѡ���� ���и������ʱȽ��У���ȷ����(����)
�����ԣ�HClO4>HBrO4>HIO4?�ڼ��ԣ�Ba(OH)2>Mg(OH)2>Be(OH)2
�������ԣ�F>C>O?�������ԣ�Li����Na����K��
����̬�⻯���ȶ��ԣ�HF��HCl��H2S
A.�٢ڢ�
B.�ڢۢ�
C.�٢ڢ�
D.�٢ڢܢ�
4��ѡ���� ������ʵ������Ľ�����ȷ����
ѡ��
| ʵ������
| ����
|
A
| Cl2ʹ���ĺ�ɫ������ɫ
| Cl2����Ư����
|
B
| NH3��HCl����Ӵ�ʱ�а��̲���
| NH3��HCl��Ӧ����NH4C1����С����
|
C
| ��Ũ�����������������
| Ũ����ʹ�����������ۻ�
|
D
| SO2ʹ�������Ƶķ�̪��Һ��ɫ
| SO2��������
|
?
5������� X��Y��Z��M��Ԫ�����ڱ���ǰ20��Ԫ�أ���ԭ����������������X��Y��Z���ڡ�X�ĺ˵������Y�ĺ����������һ�룬Y��M���γɻ�����M2Y��������������������⣺
��1��Y��Z����Ԫ�ص�����������ˮ��������___________ǿ��___________��
��2��M��Z��Y�γɵļ����ӵİ뾶�Ĵ�С________________��
��3��M2X2���������������Ӹ�����____________�������ʽΪ_______________���������к��л�ѧ����������______________��______________��
��4����Z�ĵ���ͨ��YX2��ˮ��Һ�з�����Ӧ�����ӷ���ʽΪ___________________��