1、计算题 在一定条件下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,若经还原得到的N2比经氧化得到的N2多1.4g。
(1)写出反应的化学方程式并用双线桥标出电子转移方向和数目。
(2)若以上反应进行完全,试计算原反应混合物中NO与NH3的物质的量各是多少?
参考答案:(1)“略”
(2)NO与NH3的物质的量0.15mol、0.85mol(或0.9mol、0.1mol)
本题解析:
本题难度:一般
2、选择题 向50 mL 18 mol・L-1 H2SO4溶液中加入足量的Cu片并加热,充分反应后,被还原的H2SO4的物质的量为(?)
A.小于0.45 mol
B.等于0.45 mol
C.在0.45~0.90 mol之间
D.大于0.90 mol
参考答案:A
本题解析:Cu+2H2SO4(浓)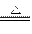 ?CuSO4+SO2↑+2H2O的反应中,有2 mol H2SO4参加反应,则有1 mol H2SO4被还原。由于Cu足量,随反应的不断进行,H2SO4由浓变稀,变成稀H2SO4后将不再与铜反应,故被还原的H2SO4的物质的量小于0.45 mol。
?CuSO4+SO2↑+2H2O的反应中,有2 mol H2SO4参加反应,则有1 mol H2SO4被还原。由于Cu足量,随反应的不断进行,H2SO4由浓变稀,变成稀H2SO4后将不再与铜反应,故被还原的H2SO4的物质的量小于0.45 mol。
本题难度:简单
3、选择题 根据下列反应判断有关物质还原性由强到弱的顺序是(?)
H2SO3+I2+H2O=H2SO4+2HI?
2FeCl3+2HI=2FeCl2+2HCl+I2
3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3
A.I- > Fe2+ > H2SO3 > NO
B.H2SO3 > I- > Fe2+ > NO
C.Fe2+ > I-> H2SO3 > NO
D.NO >Fe2+ > H2SO3 > I-
参考答案:B
本题解析:①H2SO3+I2+H2O=2HI+H2SO4中,I元素的化合价降低,S元素的化合价升高,则H2SO3为还原剂,还原性H2SO3>I-,
②2FeCl3+2HI=2FeCl2+2HCl+I2中,Fe元素的化合价降低,I元素的化合价升高,则HI为还原剂,还原性I->Fe2+,
③3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3中,N元素的化合价降低,Fe元素的化合价升高,则FeCl2为还原剂,还原性Fe2+>NO,
显然还原性由强到弱的顺序为H2SO3>I->Fe2+>NO,
故选B。
点评:本题考查氧化还原反应中还原性的比较,能利用化合价分析氧化还原反应,利用氧化还原反应中的规律来比较还原性是解答本题的关键。
本题难度:简单
4、选择题 下列过程或事实不涉及氧化还原反应的是
①蔗糖炭化?②用氢氟酸雕刻玻璃?③铁遇冷的浓硫酸钝化
④装碱液的试剂瓶不用玻璃塞?⑤雷雨发庄稼?⑥浓硝酸常显黄色
A.①③⑤⑥
B.②④
C.②④⑥
D.①②③④⑤⑥
参考答案:B
本题解析:②发生的反应为:SiO2+4HF=SiF4+2H2↑,化合价没变化,不是氧化还原反应。④发生的反应为:2NaOH+SiO2=Na2SiO3+H2O,化合价没变化,不是氧化还原反应。故选B。
点评:考查氧化还原反应的判 断,很基础的一道题。氧化还原反应是在反应前后元素的化合价具有相应的升降变化的化学反应,因此可以根据元素反应前后的化学价的变化判断反应是否为氧化还原反应。只要学生学习过程中牢记并理解这些基本定义,便不难解答此题
本题难度:简单
5、填空题 (8分)用氯气对饮用水消毒已有百年历史。这种消毒方法会使饮用水中的有机物发生氯代反应,生成有机含氯化合物,对人体有害,且氯气本身也是一种有毒气体。世界环保联盟即将全面禁止用氯气对饮用水消毒,建议推广采用广谱性高效消毒剂二氧化氯(ClO2)。目前欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,反应的化学方程式为:
___NaClO3+___HCl===___NaCl+___ClO2↑+___Cl2↑+___H2O。
(1)配平上述化学方程式。
(2)此反应中氧化剂是:__________,在反应中盐酸体现的性质是_________和_________;
(3)在标准状况下有4.48L氯气生成时,转移的电子数为_________mol,被氧化的盐酸的物质的量为________mol。
(4)我国研制成功用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2==2ClO2↑+2A。已知A物质是一种盐,它的化学式为_________。
这一方法的优点是?。
参考答案:(1)2,4,2,2,1,2.(2)NaClO3;还原性、酸性。(3)0.4;0.4。
(4)NaCl;不产生有毒的氯气,减小对环境的污染。
本题解析:考查氧化还原反应的有关判断即计算等。
(1)同一种元素之间发生氧化还原反应时,生成物的价态只能介于中间,且氧化产物的价态不能高于还原产物的价态,即ClO2是还原产物,而氯气是氧化产物,氯酸钾是还原剂,氯化氢是还原剂,所以根据电子的得失守恒可知,配平后的化学计量数依次是2,4,2,2,1,2。
(2)氯酸钾中氯元素的化合价降低,所以氯酸钾是氧化剂;盐酸中氯元素的化合价升高,所以氯化氢是还原剂。又因为还生成氯化钾,所以盐酸还起酸性的作用。
(3)标准状况下,4.48L氯气是0.2mol,则转移电子的物质的量是0.2mol×2=0.4mol,所以被氧化的盐酸就是0.4mol。
(4)根据原子守恒可知,A应该是氯化钠。根据方程式可知,该方法的优点是在反应中不能产生有毒的气体氯气。
本题难度:一般