1��ѡ���� ��ѧ������ѧϰ��ѧ����Ҫ���ߣ�����������ʾ���ʱ仯�Ļ�ѧ�����У���ȷ���ǣ�?��
A������ȼ�ϵ�صĸ�����Ӧʽ��O2 + 2H2O+ 4e- = 4OH -
B��Ǧ���س��ʱ����ʾ��+���Ľ���������Դ���������缫��ӦʽΪ��PbSO4(S)��2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq)
C����ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cu��2e- = Cu2+
D�����������绯ѧ��ʴ��������Ӧʽ��Fe��2e - = Fe2+
�ο��𰸣�B
���������A��ȼ�ϵ��ȼ���ڸ�������������Ӧ����ȼ��������������������ԭ��Ӧ������ȼ�ϵ��������������ҺΪ�����ʱ��������Ӧʽ��O2 + 2H2O+ 4e- = 4OH -������B��Ǧ���س��ʱ����ʾ��+���Ľ���������Դ���������缫��ӦʽΪ��PbSO4(S)��2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq)����ȷ��C����ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cu��2e- = Cu2+������D�����������绯ѧ��ʴ�ĸ�����Ӧʽ��Fe��2e - = Fe2+������
�����Ѷȣ���
2��ѡ���� ãã��ҹ�У������Ϊ����Աָ���˷�����Ƶĵ�Դ���볤Ч���ȶ����ҹ��Ƽ����������Ƴ������Ͻ�Pt-Fe�Ͻ���Ϊ�缫���ϵĺ�ˮ��أ������ֵ���Т����Ͻ�������?�����Ͻ��Ǹ����ۺ�ˮ�ǵ��Һ?�����Ͻ�缫������ԭ��Ӧ��˵����ȷ���ǣ�������
A���ڢ�
B���ڢ�
C���٢�
D���٢�
�ο��𰸣���ص缫ֻ��Ϊ�����������ʢٴ���
���л��õ�һ��Ϊ��������Ϊ���Ͻ𣬹ʢڶԣ�
�缫�ں�ˮ�У���ˮ�к��д����ĵ���ʣ��ʢ۶ԣ�
���Ͻ�Ϊ����������������Ӧ���ʢܴ���
��ѡA��
���������
�����Ѷȣ���
3��ʵ���� ��15�֣�������أ�K2FeO4�����и�Ч���������ã�Ϊһ�����ͷ��ȸ�Ч����������ⷨ�Ʊ�������ز�����㣬�ɹ��ʸߣ�����ʵ�����Ʊ�����ԭ������ͼ��ʾ��
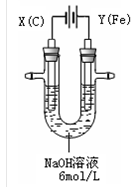
I. ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���塣�������Ϸ��֣����������FeO42��������Һ�г��Ϻ�ɫ��
��1���������У�X���� �����缫��Ӧ�� ��
��2���������У�Y���ŵ���� ��
��3�����ɸ��������FeO42�����ĵ缫��Ӧ�� ��
II. ���ò�ͬ�ֵ����Ϊ����ʵ��ĵ�Դ���������ط�Ӧ��
��1��Ǧ�����ܵĻ�ѧ����ʽΪ��
2H2O��2PbSO4 Pb��PbO2��2H2SO4�������ڳ��ʱ��������ӦΪ
Pb��PbO2��2H2SO4�������ڳ��ʱ��������ӦΪ
��
��2�����Ӽ��Գ�����ڷŵ�ʱ���������ĵ缫��Ӧ���£�
������2NiOOH��2H2O��2e����2Ni��OH��2��2OH��
������Cd��2OH����2e����Cd��OH��2
�����ڷŵ�ʱ���ܷ�Ӧ�Ļ�ѧ����ʽΪ ��
��3���£�N2H4����һ�ֿ�ȼ��Һ�壬���������ȼ�ϡ���֪��25�桢101kPaʱ��32.0g N2H4����������ȫȼ�����ɵ�����Һ̬ˮ���ų�624kJ����������N2H4��ȫȼ�յ��Ȼ�ѧ����ʽ�� ��
�¡�����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%~30%��KOH��Һ���ŵ�ʱ�����ĵ缫��Ӧ�� ��
��4���Ա���Ϊȼ����������ȼ�ϵ�أ���ص�����ͨ��O2��CO2������ͨ����飬�����������̼���Σ�����ܷ�Ӧ����ʽΪ��C3H8��5O2��3CO2��4H2O��
д���õ�������ĵ缫��Ӧ�� ��
��5�����Ʊ���ͬ���ʵ����ĸ������ʱ�������ϣ��������ֵ���зֱ����ĵ�Pb��Cd���¡���������ʵ���֮���� ��
�ο��𰸣���.��1������2H����2e��= H2������2��Fe��OH�� ��3��Fe��8OH����6e��= FeO42����4H2O
��.��1��PbSO4��2H2O��2e��= PbO2��SO42����4H��
��2��Cd��2NiOOH��2H2O = Cd��OH��2��2Ni��OH��2
��3��N2H4��1����O2��g��= N2��g����2H2O��l����H=��624kJ/mol
N2H4��4OH����4e��= 4H2O��N2��
��4��O2��2CO2��4e��= 2CO32��
��5��10:10:5:1
���������I.��1��X�͵�Դ�ĸ�����������������������Һ�е������ӷŵ磬����ʽΪ2H����2e��= H2����
��2��Y�͵�Դ������������������������Y������������ʧȥ���ӣ�����������Ӧ������ʵ��������жϣ�����������Һ�е�OH��Ҳ�ŵ�����������
��3��������ʧȥ���ӣ����������Ǹ����������ӦʽΪFe��8OH����6e��= FeO42����4H2O��
II.��1������൱�ڵ�⣬�ڵ���������ʧȥ���ӣ�����������Ӧ�����ݷ�Ӧʽ���жϣ����ʱ����Ǧʧȥ���ӣ����Ե缫��ӦʽΪPbSO4��2H2O��2e��= PbO2��SO42����4H����
��2����ԭ������������ĵ缫��Ӧʽ����Ӽ��õ��ܷ�Ӧʽ�����Է�ӦʽΪCd��2NiOOH��2H2O = Cd��OH��2��2Ni��OH��2��
��3��32.0g N2H4��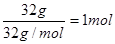 �������Ȼ�ѧ����ʽΪN2H4��1����O2��g��= N2��g����2H2O��l����H=��624kJ/mol����ȼ�ϵ���и�����ʧȥ���ӵģ��������ڸ���ͨ�룬����������Ӧ�����������ǵ�������ӦʽΪN2H4��4OH����4e��= 4H2O��N2����
�������Ȼ�ѧ����ʽΪN2H4��1����O2��g��= N2��g����2H2O��l����H=��624kJ/mol����ȼ�ϵ���и�����ʧȥ���ӵģ��������ڸ���ͨ�룬����������Ӧ�����������ǵ�������ӦʽΪN2H4��4OH����4e��= 4H2O��N2����
��4������ͨ����飬���������������CO2��ˮ�����ڵ����ˮ���ڵ�̼���Σ����Ե缫��ӦʽΪC3H8��20e����10CO32����13CO2��4H2O�������ܷ�Ӧʽ��֪��������ӦʽΪ5O2��10CO2��20e��= 10CO32����
��5��1molPb��Cd���¡�����ʧȥ�ĵ��ӷֱ�Ϊ2mol��2mol��4mol��20mol�����Ը��ݵ�ʧ�����غ��֪��Pb��Cd���¡���������ʵ���֮����10:10:5:1��
�����Ѷȣ�����
4������� �ҹ��״���������������ˮ���Ϊ��Դ�����ͺ�ˮ��־�ơ� �õ��Ժ�ˮΪ�������Һ���������е�����ʹ����������������������ֻҪ�ѵƷ��뺣ˮ�������ӣ��ͻᷢ��ҫ�۵İ⣬�������ȸɵ�ظ�20��50������ˮ�������ԣ�����ش𣺸õ�Դ����������_____��������Ҫ�ķ�Ӧ������_____���ܷ�Ӧ����Ϊ��______ ______________
______________
�ο��𰸣�
�����������
�����Ѷȣ���
5��ѡ���� �����������ڳ��ͷŵ�ʱ�����ķ�Ӧ��Fe+ NiO2+2H2O Fe(OH)2+Ni(OH)2��
Fe(OH)2+Ni(OH)2��
���и������ƶϴ�����ǣ�
�ٷŵ�ʱ��Fe���븺����Ӧ��NiO2����������Ӧ
�ڳ��ʱ�������ϵĵ缫��ӦʽΪ��Fe(OH)2 + 2e��=" Fe" + 2OH��
�۷ŵ�ʱ���������Һ�е������������������ƶ�
�ܷŵ�ʱ�������ϵĵ缫��ӦʽΪ��Fe + 2H2O��2e�� = Fe(OH)2 + 2H+
�����صĵ缫�������ij�ּ��Ե������Һ��?
A��ֻ�Т�
B���ۢ�
C���ܢ�
D���٢ڢ�
�ο��𰸣�B
����������ŵ��൱��ԭ��أ�����൱�ڵ��ء���ԭ����и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ���ڵ���������ʧȥ���ӷ���������Ӧ�������õ����ӣ�������ԭ��Ӧ������������Ӧʽ��֪������ԭ��أ������ǵ��ء���ԭ������������������ƶ������������ƶ����۲���ȷ����Ϊ�ŵ�ʱ�����������������������Һ�����������Լ��ܲ���ȷ��ӦΪFe + 2OH�D�D2e��= Fe(OH)2�����Դ���B��
�����Ѷȣ���