|
���л�ѧ֪ʶ�㽲�⡶���ᡷ����ǿ����ϰ��2017��Ѻ��棩(��)
2017-11-11 04:10:59
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1������� ���ᣨH2C2O4����һ����Ҫ�Ļ���ԭ�ϡ���֪������0��01 mol��L-l��H2C2O4��KHC2O4��K2C2O4��Һ��pH���±���ʾ��
?
| H2C2O4
| KHC2O4
| K2C2O4
| pH
| 2��0
| 3��1
| 8��1?��
|
��1����������������ʱ�����д�ʩ��ʹKHC2O4��Һ��c��K+����c��HC2O4-���ӽ�1��1����_________������ĸ����
A������������H2C2O4
B������������KHC2O4
C������������Na2C2O4
D��������Һ���¶�
| ��2��ȡһ������H2C2O4��2H2O��KHC2O4�Ļ�����ˮ�ܽ⣬���250 mL��Һ��ȡ���ݴ���Һ��25 mL�����һ����Һ���ȼ��뼸�η�̪��Һ���ٵμ�0��25  mol��L-l NaOH��Һ��20��00 mLʱ����Һ����ɫ��Ϊdz��ɫ����ڶ�����Һ�еμ�����3 mol��L-l H2S04��Һ�ữ����0��10 mol��L-l KMnO4��Һ�ζ���������KMnO4��Һ16��00 mLʱ����Һ����ɫ��Ϊdz�Ϻ�ɫ����ش��������⣺ mol��L-l NaOH��Һ��20��00 mLʱ����Һ����ɫ��Ϊdz��ɫ����ڶ�����Һ�еμ�����3 mol��L-l H2S04��Һ�ữ����0��10 mol��L-l KMnO4��Һ�ζ���������KMnO4��Һ16��00 mLʱ����Һ����ɫ��Ϊdz�Ϻ�ɫ����ش��������⣺
��������ӷ���ʽ��5C2O42-+2MnO4-+16H+��10______+2Mn2++8H2O��
��ԭ�������H2C2O4��2H2O��KHC2O4�����ʵ���֮��Ϊ__________��
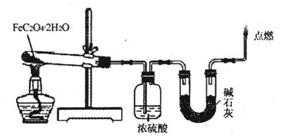
��3��ijʵ��С������ͼ��ʾ��װ��̽��FeC2O4��2H2O�ڸ����������������ȷֽ�IJ����36��0g FeC2O4��2H2O��ַ�Ӧ������������Ϊ13��6g��Ũ��������7��2g����ʯ������11��0g�����������ijɷֺ����ʵ���������֪FeC2O4��2H2O����Է�������Ϊ180���跴Ӧ���������屻������գ�
�ο��𰸣���1��AC��2�֣�?
��2����CO2��2�֣�?��1��3��2�֣�
��3�����������ΪFe��FeO�Ļ�������FeΪ0��05 mol��FeOΪ0��15 mol��4�֣������������Ϊ0��05 mol Fe4O3��Ҳ���֣�
�����������
�����Ѷȣ�һ��
2������� ijУ�о���ѧϰС�飬�������װ������֤Ũ������ľ̿�ڼ��������µIJ����к���SO2��CO2��ͬѧ�Dz������ϵ�֪���������ʹ���Ը��������Һ��ɫ����ѧ����ʽΪ��2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4
��1��д��Ũ������ľ̿�ڼ��ȵ������»�ѧ��Ӧ����ʽ��______
��2��ʵ��ʱ����Ӧ����������Ӧ��______��ͨ��װ�ã����á�a����b����գ�
��3��Aƿ��ʵ��������______��Bƿ��Һ��������______��
��4��Ҫ֤�������к���CO2��ʵ�������ǣ�C��Ʒ����Һ______��D�г���ʯ��ˮ______��
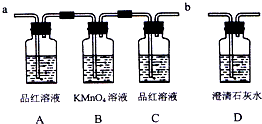
�ο��𰸣���1������ľ̿����Ũ���ᷢ����Ӧ��д��ѧ����ʽ���÷�ӦΪC+2H2SO4��Ũ����.CO2��+2SO2��+2H2O��
�ʴ�Ϊ��C+2H2SO4��Ũ����.CO2��+2SO2��+2H2O��
��2����Ӧ���ﺬ�ж�����̼�Ͷ����������壬����ʹ����ʯ��ˮ����ǣ���Ҫ����֤��������Ĵ��ڣ���ȥ������������֤������̼����Ĵ��ڣ�����ͨ����Һ������һ�������̳�������ʵ��ʱ����Ӧ����������Ӧ��a�˽���װ�ã�
�ʴ�Ϊ��a��
��3��A����֤������������Ĵ��ڣ�����������ʹƷ����Һ��ɫ��Bƿ�����Ը��������Һ���Գ�ȥ��������ѧ����ʽΪ��2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4���ڼ��������̼����ʱ���ܸ��ţ�
�ʴ�Ϊ��Ʒ����Һ��ɫ������SO2��
��4����Cװ��Ʒ�첻��ɫ��֤�������������������Dװ���г���ʯ��ˮ�����֤�����ж�����̼��
�ʴ�Ϊ������ɫ������ǣ�
���������
�����Ѷȣ���
3��ѡ���� ���й���Ũ�����������ȷ����?
[? ]
A.Ũ���������ˮ�ԣ������ʹ����̼��
B.Ũ�����ڳ����¿�Ѹ����ͭƬ��Ӧ�ų�������������
C.Ũ������һ�ָ�������ܹ����ﰱ��������������
D.Ũ�����ڳ������ܹ�ʹ�������Ƚ����ۻ�
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� Ũ������������Ҫ�����ʣ����뺬��ˮ�ֵ��������ù����в�����ʾ�������ǣ�������
A������
B����ˮ��
C��ǿ������
D����ˮ��
�ο��𰸣�A
���������
�����Ѷȣ���
5������� ��Ũ������У�A��ǿ����B��ǿ������C���߷е㡢�ѻӷ���D����ˮ��E����ˮ�Ե����ʣ����¹�����Ҫ������Ũ�������Щ���ʣ����������ĸ�ֱ���գ�
��1���ȵ�Ũ������ͭƬ��Ӧ______
��2��Ũ�������H2��O2��Cl2��HCl��SO2������______
��3��Ũ����ʹʪ�����ɫʯ����ֽ�ȱ�����______
��θ������dz�����θ��֮һ�������Ǽס������ֳ���θҩ��˵��ժҪ��
�ף���1����ɫ�ᾧ״��ĩ����ʽ�Σ���ɫ��ӦΪ��ɫ��
��2��������ˮ��ˮ��Һ�������ԣ�
��3�����������������̼��
��4��θ�����߷��ö��θ����������������θ����Σ�գ�
�ң���1�������θ�ᷢ���к����û������־ã�
��2�����������������������Ͼ��б������ã�
��3��������ϡ�������������Һ�У�
��д��������Ҫ�ɷ�����θ�����ķ�Ӧ�����ӷ���ʽ��______
��д�����е���Ҫ�ɷ�������������Һ��Ӧ�����ӷ���ʽ��______��
��д���ں�������������̼ת��Ϊ�����Ļ�ѧ����ʽ��______��
�ο��𰸣�I��1��Cu+2H2SO4��Ũ����.CuSO4+SO2��+2H2O�У�����SԪ�ػ��ϼ۲��䣬����SԪ�ػ��ϼ���+6�۱�Ϊ+4�ۣ�����Ũ�������������Ժ����ԣ���ѡAB��
��2��Ũ���������ˮ�ԣ�������������ĸ��������ѡE��
��3��Ũ����������Զ�ʹʪ�����ɫʯ����ֽ��죬Ũ���������ˮ�Զ�ʹ��ֽ��ڣ���ѡAD��
��ף���1����ɫ�ᾧ״��ĩ����ʽ�Σ���ɫ��ӦΪ��ɫ��˵��������Ԫ�أ�Ϊ��ʽ���Σ�
��2��������ˮ��ˮ��Һ�������ԣ�˵��������ʽ�������ˮ��̶ȴ��ڵ���̶ȣ�
��3�����������������̼��˵������̼Ԫ�أ�ΪΪ̼�����ƣ�
��4��θ�����߷��ö��θ����������������θ����Σ�գ�̼�����ƺ����ᷴӦ���ɶ�����̼��
�����̼�����Ʒ�Ӧ���ӷ���ʽΪ��H++HCO3-=H2O+CO2����
�ң���1�������θ�ᷢ���к����û������־ã�˵�������ʾ��������ԣ�
��2�����������������������Ͼ��б������ã����������γɽ��壻
��3��������ϡ�������������Һ�У�˵��Ϊ�����������
��������������������Һ��Ӧ����ƫ�����ƺ�ˮ�����ӷ�Ӧ����ʽΪ��Al��OH��3+OH-�TAlO2-+2H2O
���ʴ�Ϊ��H++HCO3-=H2O+CO2����Al��OH��3+OH-�TAlO2-+2H2O��
III������̼�������Ʒ�Ӧ������������Ӧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2���ʴ�Ϊ��2Na2O2+2CO2=2Na2CO3+O2��
���������
�����Ѷȣ�һ��
|  mol��L-l NaOH��Һ��20��00 mLʱ����Һ����ɫ��Ϊdz��ɫ����ڶ�����Һ�еμ�����3 mol��L-l H2S04��Һ�ữ����0��10 mol��L-l KMnO4��Һ�ζ���������KMnO4��Һ16��00 mLʱ����Һ����ɫ��Ϊdz�Ϻ�ɫ����ش��������⣺
mol��L-l NaOH��Һ��20��00 mLʱ����Һ����ɫ��Ϊdz��ɫ����ڶ�����Һ�еμ�����3 mol��L-l H2S04��Һ�ữ����0��10 mol��L-l KMnO4��Һ�ζ���������KMnO4��Һ16��00 mLʱ����Һ����ɫ��Ϊdz�Ϻ�ɫ����ش��������⣺