1、选择题 饱和一元醛和酮的混合物共0.5mol,质量为33.2g,若此混合物发生银镜反应,可析出银镜43.2g,符合题意的混合物的是(?)
A.乙醛和丙酮
B.甲醛和丙酮
C.乙醛和丁酮
D.丙醛和丁酮
参考答案:D
本题解析:混合物的平均摩尔质量为 =66.4g・mol-1,即必须有摩尔质量的数值大于66.4的物质,排除A、B项;由析出银的量可算出醛的物质的量为0.2mol,则酮的物质的量为0.3mol,排除C项,故选D项。
=66.4g・mol-1,即必须有摩尔质量的数值大于66.4的物质,排除A、B项;由析出银的量可算出醛的物质的量为0.2mol,则酮的物质的量为0.3mol,排除C项,故选D项。
本题难度:简单
2、填空题 硫酸是工业生产中最为重要的产品之一。
(1)工业上制硫酸主要分为_________、__________、__________三个阶段。
(2)下列是第二阶段反应的有关实验数据,请选择最合适的生产条件_______________。
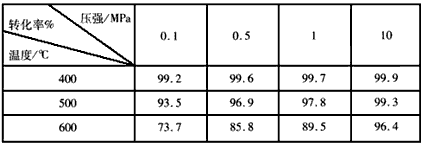
(3)现欲提高反应速率和SO2的转化率,下列措施可行的是_________(填序号)。
A.向装置中通入氮气且保持体积不变
B.向装置中通入氧气且保持体积不变
C.添加更多的催化剂
D.降低温度,及时转移SO3
(4)硫酸生产的尾气中含有少量SO2,可用石灰水吸收后,再用硫酸处理。此过程涉及的化学反应方程式为_______________________、___________________。
(5)若进入第二阶段,设备中气体的体积分数为7%SO2、11%O2、82%N2。现有100体积这样的混合气体在反应后变为96.7体积,则反应后混合气体中N2和SO3的体积比为______,此时SO2的转化率为______。
参考答案:(1)造气;催化氧化;吸收
(2)400℃、0.1MPa(或常压)
(3)B
(4)SO2+Ca(OH)2=CaSO3↓+H2O;CaSO3+H2SO4=CaSO4+SO2↑+H2O
(5)410:33(或82:6.6);94.3%
本题解析:
本题难度:一般
3、填空题 工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
(1)氨催化氧化的化学方程式为_________________:
(2)原料气中空气必须过量,其主要原因是_________________;
(3)将铂铑合金做成薄丝网的主要原因是________________;
(4)水吸收二氧化氮生成硝酸为放热反应,其化学方程式为_________________________,为了提高水对二氧化氮的吸收率,可采取的措施为_____________________________(答2项)。
参考答案:(1)4NH3+5O2 4NO+6H2O?
4NO+6H2O?
(2)提高氨的转化率和一氧化氮的转化率
(3)增大单位质量的催化剂与反应物的接触面积
(4)3NO2+H2O=2HNO3+NO;加压、降温
本题解析:
本题难度:困难
4、选择题 浓硫酸可用铁制的槽运输是因为
A.常温下铁与硫酸根本不反应
B.浓硫酸能使铁的表面生成氧化物保护膜
C.浓H2SO4电离出很少的H+
D.密闭容器中无空气
参考答案:B
本题解析:对钝化的解释,是生成致密的氧化膜,阻止反应进一步进行.
本题难度:简单
5、选择题 下列应用化学学科研究物质性质的基本方法或所得结论中,不正确的是( )
A.根据物质的元素组成,将纯净物分为单质和化合物
B.通过钠、镁、铝与水反应的实验,比较三种单质的金属性
C.根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不会与浓硫酸发生反应
D.打开盛装浓氨水的试剂瓶塞,观察现象,了解氨的某些物理性质
参考答案:A.由同种元素组成的纯净物为单质,由不同种元素组成的纯净物为化合物,故A正确;
B.金属性:钠>镁>铝,单质的金属性越强,与水反应越剧烈,故B正确;
C.常温下铝与浓硫酸发生钝化反应,可用铝质容器储存浓硫酸,故C错误;
D.氨水易挥发,有刺激性气味,打开盛装浓氨水的试剂瓶塞,可闻到刺激性气味并能观察到白雾现象,故D正确.
故选C.
本题解析:
本题难度:一般