1、选择题 向浓度相同的Al2(SO4)3、(NH4)2Fe(SO4)2、MgSO4溶液中,加入等体积等浓度的BaCl2溶液时,恰好使上述三种溶液中SO42-全部沉淀,则Al2(SO4)3、(NH4)2Fe(SO4)2、MgSO4三种盐溶液的体积之比为( )
A.1:2:3
B.3:2:1
C.2:3:6
D.6:3:2
2、计算题 (10分)“铜都”安徽铜陵有许多黄铜矿(主要成分为CuFeS2,含少量Al2O3、SiO2),黄铜矿是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2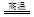 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是 (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为 L。
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是 (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为 L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式 ,该反应中稀硝酸体现 & #160; (填“氧化性”、“还原性”或“酸性”)。
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0mol?L-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为 。
3、填空题 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)利用反应:6NO2+8NH3 7N2+12H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是 L。
7N2+12H2O可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下的体积是 L。
(2)①已知:2SO2(g)+O2(g) 2SO3(g) ΔH=?196.6 kJ・mol
2SO3(g) ΔH=?196.6 kJ・mol
4、选择题 下列化学用语使用正确的是(?)
A.F-离子的结构示意图: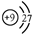
B.水分子的球棍模型:
C.HCN分子的结构式:H―C≡N
D.二氧化碳的电子式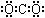
5、填空题 (3分)酸性条件下,许多氧化剂可使KI溶液中的I-氧化,例如KIO3(IO3-→I2)、H2O2(H2O2→H2O)、FeCl3(Fe3+→Fe2+)、K2Cr2O7(Cr2O72-→Cr3+)。请根据题目要求填空:
(1)写出在醋酸存在的条件下KIO3溶液与KI溶液反应的离子方程式 。
(2)在酸性条件下(足量),各取1 L浓度为1 mol・L-1的KI溶液分别与上述列举四种溶液进行完全反应,则需要溶质的物质的量之比为n(KIO3):n(H2O2):n(FeCl3):n(K2Cr2O7)=" " : : : .(要求写出最简比)