1、选择题 已知某物质X能发生如下转化:
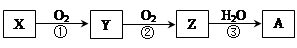
下列有关上述转化关系中物质及其反应的叙述错误的是
A.若X为N2或NH3,则A为硝酸
B.若X为S或H2S,则A为硫酸
C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
参考答案:D
本题解析:N2或NH3可以被O2氧化为NO,NO可被O2氧化为NO2,NO2与H2O反应生成硝酸和NO,故A项正确;S或H2S可以被O2氧化为SO2,SO2可被O2氧化为SO3,SO3与H2O反应生成硫酸,故B项错误;稀硝酸与铜能反应生成NO,稀硫酸与铜不反应,浓硝酸与铜反应生成NO2,浓硫酸与铜加热反应生成SO2,故C项错误;NO2与H2O反应是氧化还原反应,SO3与H2O反应是非氧化还原反应,故D项正确。
本题难度:一般
2、选择题 有些化学反应不仅与反应物种类有关,还与反应条件(反应温度、反应物浓度)或反应物物质的量的比值有关,下列反应中与反应条件(反应温度、反应物浓度)、反应物物质的量的比值无关的是( )
A.Fe粉与Cl2气
B.CO2与Ca(OH)2溶液
C.Zn与H2SO4
D.Na2CO3与H2SO4溶液
参考答案:A、铁在氯气中燃烧,无论铁是否过量,产物都是氯化铁,故A正确;
B、CO2与Ca(OH)2溶液反应,当CO2少量时生成碳酸钙,CO2过量时生成碳酸氢钙,故B错误;
C、Zn与浓H2SO4反应生成二氧化硫,和稀H2SO4反应生成氢气,所以与浓度有关,故C错误;
D、Na2CO3与H2SO4溶液反应,硫酸少量生成NaHCO3,硫酸过量生成CO2,故D错误;
故选A.
本题解析:
本题难度:一般
3、选择题 实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是(? )
A.由题目信息知:KMnO4的氧化性比MnO2的强
B.制备氯气的整个实验过程中,只需要使用氧化剂与还原剂
C.用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体
D.用足量MnO2与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol
参考答案:B
本题解析:比较反应的条件即可说明KMnO4的氧化性强于MnO2;因氯气有毒,需要用碱溶液吸收尾气;当整个集气瓶充满黄绿色时表明已收集满了;浓盐酸变稀后不与MnO2反应,生成氯气的物质的量小于1 mol。
本题难度:一般
4、选择题 在反应8NH3+3Cl2====6NH4Cl+N2中,被氧化的NH3与未被氧化的NH3的质量之比为
A.3:8
B.8:3
C.1:3
D.3:1
参考答案:C
本题解析:被氧化的NH3即为转化成N2的NH3,未氧化的氨即为转化成NH4Cl的NH3.故它们的比例应为:2:6=1:3,即C正确.
本题难度:一般
5、选择题 下列有关物质的性质或用途的说法中,正确的是
① 氯气具有漂白性,可以直接使有色布条褪色;② 二氧化硫具有较强的还原性,不能用浓硫酸干燥;③ Zn具有还原性和导电性,可用作锌锰干电池的负极材料;
④ 是两性氢氧化物,能溶于强酸或强碱。
是两性氢氧化物,能溶于强酸或强碱。
A.①②③
B.②③④
C.③④
D.①②④
参考答案:C
本题解析:①干燥的氯气不具备漂白性,具有漂白性的是次氯酸,故错误。②二氧化硫中硫元素处于中间价态,具有还原性,而浓硫酸具有氧化性,因此二者可以发生反应,故正确。③常用的锌锰干电池的负极材料为锌,故正确。④氢氧化铝具有两性,能与强酸或强碱发生反应,故正确。综上,答案选C。
点评:对物质的性质与用途属于化学的基础内容,解题的关键在于熟练掌握相关物质的性质以及其对应的化学方程式。
本题难度:简单