1、选择题 将过量的CO2通入下列溶液中,最终出现浑浊的是
A.CaCl2溶液
B.石灰水?
C.饱和Na2CO3溶液
D.水玻璃
参考答案:CD
本题解析:同温下NaHCO3比Na2CO3的溶解度要小。?
本题难度:一般
2、计算题 有一铅锡合金质量为100g,完全氧化后得到氧化物的混合物质量为116g,求合金中铅、锡的质量分数各为多少?
参考答案:合金中铅、锡分别占56.8%、43.2%
本题解析:解法一:
分析:设100g铅锡合金中含锡xg,则含铅(100-x)g。①Sn氧化后的稳定产物是SnO2(+4价氧化物稳定),Sn的相对原子质量为

Pb氧化后的稳定产物是PbO(+2价氧化物稳定), Pb的相对原子质量为207,PbO的式量为223,(100-x)g Pb氧化生成的PbO质量必
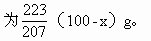
因为SnO2与PbO质量共为116g,故可列一元一次方程,解方程求出Sn、Pb质量。
[解] 设100g锡铅合金中含锡xg,含铅为(100-x)g。
根据化学式所表示的元素质量分数及题意,列代数方程式:
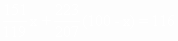
解得x=43.2(g)
100-x=100-43.2=56.8(g)

答:合金中锡、铅质量分数分别为43.2%、56.8%
解法二:
分析:此题利用物质的量计算也很方便。设100g合金中含xg,含铅为(100-x)g
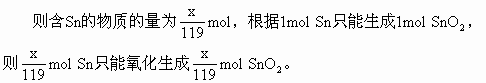

将SnO2与PbO由物质的量换算成质量,质量和为116g。
解:设100g锡铅合金中含锡为xg,含铅为(100-x)g
Sn的物质的量=SnO2的物质的量

Pb的物质的量=PbO的物质的量

SnO2与PbO质量和为116g
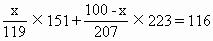
解得 x=43.2(g)
(锡的质量)
100-x=56.8(g)
(铅的质量)
本题难度:简单
3、选择题 下列离子方程式书写正确的是(? )
A.碳酸氢钙溶液中加入盐酸 +H+
+H+ CO2↑+H2O
CO2↑+H2O
B.碳酸氢钙溶液中加入足量的氢氧化钠溶液Ca2++OH-+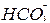
 CaCO3↓+H2O
CaCO3↓+H2O
C.稀硫酸和氢氧化钡溶液混合Ba2++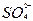
 BaSO4↓
BaSO4↓
D.水玻璃中通入足量二氧化碳 +H2O+CO2
+H2O+CO2
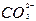 +H2SiO3↓
+H2SiO3↓
参考答案:A
本题解析:
B项应为Ca2++2OH-+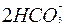
 CaCO3↓+H2O+
CaCO3↓+H2O+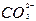 。
。
C项应为:Ba2++2OH-+2H++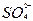
 BaSO4↓+2H2O。?
BaSO4↓+2H2O。?
D项应为: +2H2O+2CO2
+2H2O+2CO2
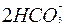 +H2SiO3↓
+H2SiO3↓
本题难度:一般
4、选择题 人类已进入信息化社会,光导纤维是传递信息的必不可少的材料。光导纤维属于
A.无机非金属材料
B.金属材料
C.有机高分子材料
D.复合材料
参考答案:A
本题解析:考查化学与生活、生产等。光导纤维主要是二氧化硅,属于无机非金属材料,答案选A。
本题难度:简单
5、选择题 在密闭容器中充入CO2和CO的混合气体,其密度是相同条件下氦气密度的8倍,这时测得容器内的压强为p1。若控制容器的体积不变,加入足量的Na2O2,充分振荡并不断用电火花点燃至完全反应,恢复到开始时的温度,再次测得容器内的压强为p2,则p1和p2的关系是(? )
A.p1=8p2
B.p1=4p2
C.p1=2p2
D.p1=p2
参考答案:A
本题解析: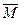 =8×4=32
=8×4=32

n(CO2)∶n(CO)=1∶3
由2CO2+2Na2O2====2Na2CO3+O2
2CO+O2====2CO2
将上述二式合并得Na2O2+CO====Na2CO3
假设CO2、CO分别有1 mol、3 mol,3 mol CO最终将完全被吸收,1 mol CO2变为0.5 mol O2,则:
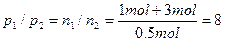 。
。
本题难度:简单