|
|
|
高考化学知识点总结《化学反应速率》高频试题强化练习(2017年最新版)(一)
2017-11-11 04:18:49
来源:91考试网
作者:www.91exam.org 【 大 中 小】
3、填空题 (11分)甲醇可作电池的原料,也会造成环境污染。请根据有关反应回答问题。
(1)以CH4和H2O为原料,通过下列反应可制备甲醇。
①CH4(g)+H2O(g)?CO(g)+3H2(g) △H =+206.0 kJ・mol-1
②CO(g)+2H2(g)?CH3OH (g) △H=-129.0 kJ・mol-1
则CH4(g)+H2O(g) ?CH3OH (g)+H2(g)的△H= kJ・mol-1。
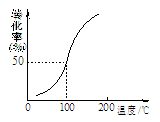
(2)将1.0 mol CH4(g)和2.0 mol H2O(g)通入容积为10 L的容器,在一定条件下发生反应①,测得在一定压强下CH4的转化率与温度的关系如图。设100℃时达到平衡所需的时间为5 min,
则这时间段v(H2)= mol・L-1・min-1。
(3)在一定温度下,将一定量CO和H2充入密闭容器发生反应②。达到平衡后,若压缩容器体积至原来的 ,对平衡体系产生的影响是 (填序号)。 ,对平衡体系产生的影响是 (填序号)。
①c ( H2 )减小 ②CH3OH 的物质的量增加 ③新平衡时, 减小, 减小,
④正反应速率加快,逆反应速率减慢 ⑤平衡常数K增大
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用下图装置模拟上述过程,则:

①Co2+在阳极的电极反应式为 ;
②请完成除去甲醇的离子方程式:Co3++CH3OH+ = Co2++CO2↑+6H+
4、选择题 一定能使化学反应NaOH+HCl====NaCl+H2O速率加快的方法是( )
(a)升温 (b)减小生成物浓度 (c)增加反应物浓度 (d)加压
A.(a)(b)和(c)
B.(a)和(c)
C.(b)和(d)
D.全部
|
5、选择题 在恒容密闭容器进行的可逆反应:MgSO4(s) + CO(g)  ?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
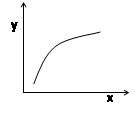
A.若平衡常数K值变大,平衡移动时v逆先减小后增大
B.容器中固体物质的质量不再改变,则反应到达平衡状态
C.若x表示温度,y可表示平衡时混合气体的密度
D.若x表示CO物质的量,y可表示平衡时CO2与CO物质的量之比
 ?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是
?MgO(s) + CO2(g) + SO2(g)-Q,下列分析合理的是