1、填空题 (14分)镁是海水中含量较多的金属,镁合金及其镁的化合物用途非常广泛。
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(S) △H1="-" 74.5kJ・mol-1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2="-" 64.4kJ・mol-l
则:Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)的△H3= .
(2)某科研小组用水氯镁石(主要成分为MgCl2・6H2O)制备金属镁工艺的关键流程如下:
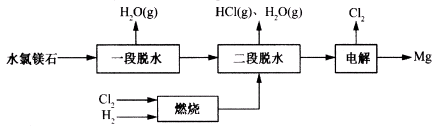
科研小组将MgCl2・6H2O在氩气气氛中进行热重分析,结果如下图(TG表示残留固体质量占原样品总质量的百分数)。
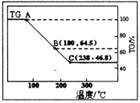
①图中AB线段为“一段脱水”,试确定B点对应固体物质的化学式____ ;图中BC线段为“二段脱水”,在实验中通入H2和Cl2燃烧产物的目的是 。
②该工艺中,可以循环使用的物质有___ 。
(3)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是 ,该化合物水解时生成甲烷、氯化镁和氢氧化镁,请写出该反应的化学方程式 。
(4)储氢材料Mg(AIH4)2在110~200℃的反应为:Mg(AIH4)2=MgH2+2Al+3H2↑;每转移3 mol电子生成Al的质量为____ 。
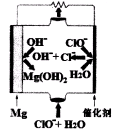
(5)“镁一次氯酸盐”燃料电池的装置如右图所示,该电池的正极反应式为 。
参考答案:本题共14分,除注明以外,每空2分 (1)+84.6kJ/mol
(2)①MgCl2・2H2O;为防止MgCl2・2H2O脱水过程中发生水解反应(1分) ②HCl,Cl2
(3)+2(1分),2CH3MgCl +2H2O→Mg(OH)2+MgCl2+2CH4↑(写等号也可)
(4)27g (5)ClO-+2e-+H2O=Cl-+2OH-
本题解析:(1)已知:①Mg(s)+H2(g)=MgH2(S) △H1=―74.5kJ・mol-1,②Mg2Ni(s)+2H2(g)=Mg2NiH4(s) △H2=―64.4kJ・mol-l,则根据盖斯定律可知②―①×2即可得到Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)的△H3=+84.6kJ/mol。
(2)①设原样品是1mol,质量是203g,B点剩余固体的质量是203g×0.646=131g,即固体减少了72g,恰好是4mol水的质量,所以此时固体的化学式为MgCl2・2H2O。由于镁氯化水解生成氢氧化镁和氯化氢,加热能促进镁离子水解,所以为防止MgCl2・2H2O脱水过程中发生水解反应,需要在实验中通入H2和Cl2燃烧产物氯化氢。
②二段脱水时产生氯化氢,以及电解时生成的氯气均可以循环使用。
(3)CH3MgCl是一种重要的有机合成剂,其中C、H、Cl的化合价分别是―4价、+1价和―1价,所以根据化合物中化合价代数和为0可知镁的化合价是+2价。该化合物水解时生成甲烷、氯化镁和氢氧化镁,因此该反应的化学方程式为2CH3MgCl +2H2O→Mg(OH)2+MgCl2+2CH4↑。
(4)根据方程式Mg(AIH4)2=MgH2+2Al+3H2↑可知铝元素的化合价从+3价降低到0价,失去3个电子,则每转移3 mol电子生成1molAl,其质量为27g。
(5)原电池中正极得到电子,发生还原反应,则根据装置图可知负极镁失去电子,正极次氯酸根得到电子,因此该电池的正极反应式为ClO-+2e-+H2O=Cl-+2OH-。
考点:考查盖斯定律、盐类水解、氧化还原反应、原电池以及制备流程图分析
本题难度:困难
2、选择题 下列有机化学方程式书写正确的( )
A.CH4+Cl2
CH2Cl2+H2
B.H2C=CH2+Br2→CH3CHBr2
C.CH3CH2OH+CH3COOHCH3COOCH2CH3
D.2CH3CH2OH+O22CH3CHO+2H2O
参考答案:D
本题解析:
本题难度:一般
3、选择题 将维生素C溶液滴入氯化铁溶液中,可观察到氯化铁溶液的黄色褪去,这说明维生素C? (? )
A.有较强氧化性
B.有较强还原性
C.既有氧化性,又有还原性
D.遇热易分解
参考答案:B
本题解析:
正确答案:B
Fe3+ 有较强的氧化性,氯化铁溶液的黄色褪去,被还原,这说明维生素C有较强还原性
本题难度:简单
4、选择题 有关碳元素及其化合物的化学用语正确的是
A.CO2的电子式: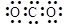
B.C原子最外层电子的轨道表示式: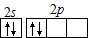
C.醋酸钠的分子式:C2H3O2Na
D.乙烯的比例模型:
参考答案:D
本题解析:A、碳与氧之间共有两对电子,错误;B、根据保利原理和洪特规则,先占据更多的轨道,错误;C、醋酸钠为盐,离子化合物,不存在分子式,错误;D、正确。
本题难度:一般
5、选择题 在NO2与H2O的反应中,发生还原反应和发生氧化反应的物质的质量比为(?)。
A.3:1
B.1:3
C.1:2
D.2:1
参考答案:C
本题解析:3 NO2 +H2O=2HNO3 +NO,NO2与水发生岐化反应,3个N原子中有两个N自+4价升高至+5价,另一下降低至+2价,故答案为C
本题难度:一般