1������� �����£���һ���������ڲ���һ����©���ҿ��Ի����Ļ������������ָ���������ң����ҳ���N2�����ҳ���H2��O2����������ʹN2ռ���������
����ͼ����Ȼ���ȼH2��O2�Ļ�����壬��Ӧ��Ϻ�ָ���ԭ�����¶ȣ���������ͣ�����������м䣮�����飬��ʱ�����������ʹ�����ǵ�ľ����ȼ����ӦǰH2��O2�����ʵ���֮��Ϊ______�������Ҫд��������̣�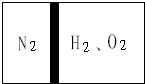
�ο��𰸣��赪�������ʵ���Ϊ1mol��
���ҳ���N2�����ҳ���H2��O2����������ʹN2ռ���������14��
����ѹǿ��ȣ���������ʵ���֮�ȵ������֮�ȣ�
��H2��O2�����ʵ���Ϊ3mol��
��ȼH2��O2�Ļ�����壬��Ӧ����ʽΪ2H2+O2?��ȼ?.?2H2O��
��Ӧ���������ͣ�����������м䣮˵����Ӧ��������������ʵ�����ȣ�
�����������ʹ�����ǵ�ľ����ȼ��ʣ������Ϊ1mol��
��Ӧ��H2��O2��Ϊ2mol������n��H2��=43mol��n��O2��=23mol��
����ԭ������n��H2��=43mol��n��O2��=23mol+1mol=53mol��
��ӦǰH2��O2�����ʵ���֮��Ϊ43��53=4��5��
�ʴ�Ϊ��4��5��
���������
�����Ѷȣ�һ��
2��ѡ���� �칬һ�Ŵ��صij������Ż��ʹ�õ���Ҫȼ����ƫ�����£���R��ʾ�����������������ڻ������ʱ�����߾��ҷ�Ӧ�����������岢�ͷų��������ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ��R + 2N2O4��3N2?+ 4H2O + 2CO2�����������������
A���˷�Ӧ����˲����������������壬�ƶ��������
B���˷�Ӧ��������ԭ��Ӧ��N2O4����ԭ��
C���˷�Ӧ��������ԭ��Ӧ��ƫ����������ԭ��
D���˷�Ӧ��R�ķ���ʽΪC2H8N2
�ο��𰸣�B
���������A��ƫ�����º��������������ҷ�Ӧ�����������岢�ͷų��������ȣ�˲����������������壬�ƶ�������У���A��ȷ��B��NԪ���ڷ�Ӧ�����Ի���̬���ڣ���Ӧ���ɵ�����NԪ�ػ��ϼ۱仯����˸÷�Ӧ��������ԭ��Ӧ��N2O4��NԪ�ػ��ϼ۴ӣ�4�۽��͵�0�ۣ�N2O4������������B����C��N2O4��NԪ�ػ��ϼ۽��ͣ�N2O4����������ƫ������������Ԫ�ػ��ϼ�һ�������ߣ���ƫ����������ԭ������C��ȷ��D������ԭ���غ��֪��ƫ�����µķ���ʽΪC2H8N2����D��ȷ����ѡB��
�����Ѷȣ���
3��ѡ���� ��������ȵ�����2%ת��Ϊ�����Լ�ǿ�ġ��������������ܼ�������˥�ϣ�����Ϊ������ɱ�֡������ú���Ԫ�صĻ������������ƣ�Na2SeO3��������������ȵĻ��������ɴ��ƶ�Na2SeO3��������
A������ԭ��
B����������
C������������������ԭ��
D���Ȳ����������ֲ�����ԭ��
�ο��𰸣�A
���������������ԭ��Ӧ�У���ԭ��+����������������+��ԭ�����ԭ�����л�ԭ�ԣ�����������ԭ�ɻ�ԭ������������������Լ�ǿ�����ú���Ԫ�أ�Se���Ļ������������ƣ�Na2SeO3��������������ȵĻ�����������Na2SeO3�ܽ�������������ԭ������������Ϊ��������Na2SeO3Ϊ��ԭ�������Դ�ѡA��
�����Ѷȣ���
4��ѡ���� ��5ml0.05mol/L��ij�����Ȼ������Һ�У��μ�
0.1mol/LAgNO3��Һ�����ɳ��������������AgNO3��Һ�������ϵ��ͼ��ʾ������Ȼ����н���Ԫ�صĻ��ϼ�Ϊ
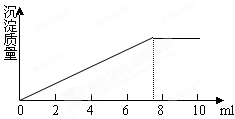
A��+1
B��+2
C��+3
D��+4
�ο��𰸣�C
���������
���������������Ӻ�������֮�䷴Ӧ�����Ȼ���������ʵ���Լ��Ȼ���Ļ�ѧʽ���м��㣮
��𣺽⣺�Ȼ����ֵ�Cl-��Ag+1��1��Ӧ��������ĵ��������������ʵ���Ϊ��Щ��Һ��Cl-���ӵ����ʵ�����n��Cl-��=n��Ag+��=7.5��10-3L��0.1mol/L=7.5��10-4mol��
��ý����Ļ��ϼ�ΪX�仯ѧʽΪA��Cl��x��n��Ax+��=5��10-3L��0.05mol/L=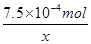 �����x=3��
�����x=3��
��ѡC��
���������⿼��ѧ�������ͽ���������������һ���й����ӷ�Ӧ�ļ����⣬�ѶȲ���
�����Ѷȣ���
5��ѡ���� ���л�ѧ������ȷ���ǣ�?��
A����ϩ�Ľṹ��ʽ��CH2CH2
B��CO2�ĵ���ʽ��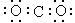
C���Ȼ�þ�ĵ���ʽ��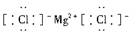
D��K���Ľṹʾ��ͼ��
�ο��𰸣�C
����������ṹ��ʽӦ�����ֹ����ţ�������ϩ�Ľṹ��ʽΪCH2��CH2��A����ȷ��CO2�����к���̼��˫��������ʽΪ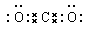 ��B����ȷ�������ӵ���������19��D����ȷ��������ȷ�Ĵ�ѡC��
��B����ȷ�������ӵ���������19��D����ȷ��������ȷ�Ĵ�ѡC��
�����Ѷȣ���