1、选择题 为保护地下钢管不受腐蚀,可使它与(? )
①直流电源负极相连?②铜板相连
③锌板相连?④直流电源正极相连
A.①②
B.③④
C.①③
D.②④
参考答案:C
本题解析:本题考查的是金属的电化学防护方法:①外加电流阴极保护法:把金属连接在电源的负极上,这样就能消除引起金属腐蚀的原电池反应;②牺牲阳极保护法:在金属上铆接比它更活泼的另一金属,发生金属腐蚀而金属本身受到保护。所以选①③,C正确。
本题难度:简单
2、选择题 下列装置中(杯中均盛有海水)能使铁受到保护不被腐蚀的是
[? ]
A.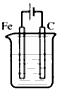
B.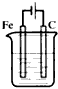
C.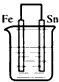
D.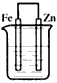
参考答案:B
本题解析:
本题难度:一般
3、选择题 关于下图装置中的变化叙述错误的是
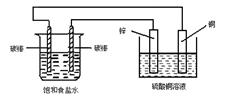
A.电子从锌片流向右侧碳棒,再从左侧碳棒流回铜片
B.锌片上发生氧化反应
C.左侧碳棒上发生:2H2O+O2+4e→4OH-
D.铜电极析出铜
参考答案:C
本题解析:A、锌片为电池的负极,正确;B、锌失电子发生氧化反应, 正确;C、左侧碳棒上发生:2Cl? - 2e?=Cl2↑,错误;D、铜电极发生铜离子得电子生成铜的反应。
本题难度:一般
4、选择题 如图,缠上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到在金属条表面的溶液出现粉红色。该金属条可能是? ( )。
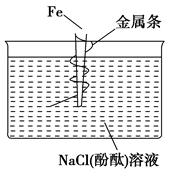
A.铜
B.镁
C.铝
D.锌
参考答案:A
本题解析:出现粉红色说明金属条附近产生了OH-,发生了吸氧腐蚀,金属条作正极,其活泼性比铁要差。
本题难度:简单
5、选择题 如图装置进行实验,关于此装置,下列的叙述正确的是
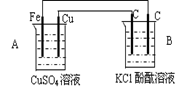
A.A池是电解池
B.Fe极是阴极
C.B池是原电池
D.B池溶液变红
参考答案:D
本题解析:A符合原电池的构成条件:1、有活动性不同的电极,2、有电解质溶液,3、有闭合回路,4、有自发的氧化还原反应。所以A是原电池。则B为电解池。A中铁的活动性大于铜,所以铁做负极。 B中电解氯化钾溶液产生氢氧化钾,使酚酞变红。所以D正确。
点评:掌握着两种电化学装置的特点。电极名称、电极反应,不难判断。
本题难度:一般