1、填空题 (6分)写出下列物质间反应的离子方程式:
(1)氯化铝溶液中加入过量氨水?;
(2)氢氧化钡溶液与硫酸铜溶液混合?;
(3)少量NaHSO4溶液与过量氢氧化钡溶液?。
2、填空题 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感。
(1)过碳酸钠是一种有多种用途的新型氧系固态漂白剂,化学式可表示为Na2CO3・3H2O2,它具有Na2CO3和H2O2的双重性质。
①H2O2有时可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O=A+NH3↑,则生成物A的化学式______________
②某强酸性反应体系中,反应物和生成物共六种物质:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→ O2。
写出该反应的离子方程式:_______________________________________________。
(2)某天然碱的化学式可表示为:aNa2CO3・bNaHCO3・2H2O,取m g天然碱溶于水配成溶液,再向溶液中逐滴加入1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系某同学作出了如图所示的A和B曲线,试回答下列问题:
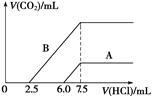
①_______曲线正确,天然碱的化学式为___________,
②加盐酸后产生CO2气体体积(标准状况)的最大值为? _____________mL。
(3) 常温下用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2可生成0.5 mol N2,则y=_______________。
3、选择题 下列离子方程式的正误判断及评价均正确的是
?
| 离子反应
| 离子方程式
| 判断及评价
|
A
| 在NH4HCO3溶液中加少量NaOH加热
| NH4++OH- =NH3・H2O
| 错误,加热条件下应生成氨气
|
B
| 在FeI2溶液中加少量的溴水
| 2I-+Br2=I2+2Br-
| 正确,还原性I-大于Fe2+
|
C
| 在NaAlO2溶液中通入少量的CO2气体
| 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
| 错误,应生成HCO3-
|
D
| 在稀硝酸中加入少量的铁粉
| 3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
| 正确,稀硝酸的还原产物为NO
|
?
4、选择题 下列离子方程式书写正确的是
[? ]
A.铝片放入NaOH溶液中:2Al + 2OH-= 2AlO2- + H2↑
B.碳酸钙溶于醋酸中:CaCO3 + 2H+= Ca2+ + CO2↑+ H2O
C.氯气通入NaOH稀溶液中:Cl2 + 2OH-= Cl-+ ClO-+ H2O
D.Ba(OH)2溶液与过量NaHSO4溶液混合:H+ + SO42-+ Ba2+ + OH-= BaSO4↓+ H2O
5、填空题
Ⅰ.高铁酸钾(K2FeO4)是极好的氧化剂,具有高效的消毒作用,为一种新型非氯高效消毒剂。其生产工艺流程如下:
 ?
?
请同答下列问题。
(1)写出向KOH溶液中通入足量Cl2发生反应的离子方程式?。
(2)在溶液I中加入KOH固体的目的是?(选填序号)。
A.为下一步反应提供碱性的环境
B.使KClO3转化为KClO
C.与溶液I中过量的Cl2继续反应,生成更多的KClO
D.KOH固体溶解会放出较多的热量,有利于提高反应速率和KClO的纯度
 3Zn+2K2FeO4+8H2O,
3Zn+2K2FeO4+8H2O,