1、选择题 下列叙述正确的是
A.pH相等的CH3COONa、NaOH和Na2CO3三种溶液浓度大小关系为:c(NaOH)<c(CH3COONa)<c(Na2CO3)
B.0.1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
C.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
D.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
参考答案:D
本题解析:等浓度的CH3COONa溶液和Na2CO3溶液,由于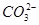 的水解程度大于CH3COO-的水解程度,Na2CO3溶液的碱性强于CH3COONa溶液的碱性,故等pH的两溶液,CH3COONa溶液的浓度大,A项错误;0.1 mol/L NaHA溶液的pH=4,说明溶液中存在HA-的电离和水解,且电离程度大于水解程度,电离产生H+和A2-,水解产生H2A和OH-,故c(A2-)>c(H2A),B项错误;使醋酸的pH增大1,需要将醋酸稀释的倍数要远大于10倍,C项错误;pH=11的NaOH溶液中c(OH-)=10-3 mol・L-1,pH=3的醋酸溶液中c(H+)=10-3 mol・L-1,但醋酸的浓度远大于NaOH溶液的浓度,二者等体积混合后醋酸过量,溶液呈酸性,滴入石蕊溶液呈红色。
的水解程度大于CH3COO-的水解程度,Na2CO3溶液的碱性强于CH3COONa溶液的碱性,故等pH的两溶液,CH3COONa溶液的浓度大,A项错误;0.1 mol/L NaHA溶液的pH=4,说明溶液中存在HA-的电离和水解,且电离程度大于水解程度,电离产生H+和A2-,水解产生H2A和OH-,故c(A2-)>c(H2A),B项错误;使醋酸的pH增大1,需要将醋酸稀释的倍数要远大于10倍,C项错误;pH=11的NaOH溶液中c(OH-)=10-3 mol・L-1,pH=3的醋酸溶液中c(H+)=10-3 mol・L-1,但醋酸的浓度远大于NaOH溶液的浓度,二者等体积混合后醋酸过量,溶液呈酸性,滴入石蕊溶液呈红色。
本题难度:一般
2、选择题 有人欲配制下列含有四种不同阴、阳离子的溶液,其中能配制成功的是( )
A.Fe2+、OH-、H+、Cl-、NO3-
B.Ca2+、H+、Cl-、CO32-
C.Mg2+、Al3+、Cl-、SO42-
D.Na+、Ba2+、NO3-、SO42-
参考答案:A.因Fe2+、OH-结合生成沉淀,OH-、H+结合生成水,则不能成功,故A错误;
B.因Ca2+、CO32-结合来源:91考试网 www.91eXam.org生成沉淀,H+、CO32-结合生成水和气体,则不能成功,故B错误;
C.因该组离子之间不反应,能配制成功,故C正确;
D.因Ba2+、SO42-结合生成沉淀,则不能成功,故D错误;
故选C.
本题解析:
本题难度:一般
3、选择题 常温下,由水电离出的氢离子浓度为1×10-13mol/L的溶液中,一定不能大量共存的离子组是( )
A.Cl-AlO2-Na+K+
B.Mg2+NO3-Br-K+
C.Fe2+Cl-Ba2+Cl-
D.SO32-Na+S2-K+
参考答案:A、若是酸的溶液,则H+与AlO2-反应,若是碱的溶液,该组离子之间不反应,即可能大量共存,故A不选;
B、若是酸的溶液,则H+与NO3-、Br-发生氧化还原反应,若是碱的溶液,OH-与Mg2+反应生成沉淀,即一定不能大量共存,故B选;
C、若是碱的溶液,OH-与Fe2+反应生成沉淀,若是酸的溶液,则该组离子之间不反应,即可能大量共存,故C不选;
D、若是酸的溶液,则H+与SO32-、S2-发生氧化还原反应,若是碱的溶液,该组离子之间不反应,即可能大量共存,故D不选;
故选B.
本题解析:
本题难度:简单
4、实验题 (6分)某同学进行如下实验:
向盛有10滴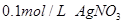 溶液的试管中滴加
溶液的试管中滴加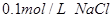 溶液,至不再有白色沉淀生成。向其中滴加
溶液,至不再有白色沉淀生成。向其中滴加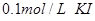 溶液;再向其中滴加
溶液;再向其中滴加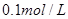 的
的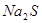 溶液。
溶液。
请回答:
(1)白色沉淀是 ,证明“不再有白色沉淀生成”的操作是 。
(2)能说明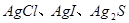 溶解度依次减小的现象为 。
溶解度依次减小的现象为 。
(3)滴加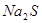 溶液后发生反应的离子方程式是 。
溶液后发生反应的离子方程式是 。
参考答案:(1)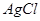 1分
1分
静置后取上层清液,加入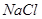 溶液,若不出现白色沉淀,证明
溶液,若不出现白色沉淀,证明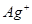 已经沉淀完全。
已经沉淀完全。
(表述合理即可得分) 1分
(2)白色沉淀转化为黄色,黄色沉淀转化为黑色 2分
(3)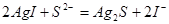 2分
2分
本题解析:(1)硝酸银和氯化钠反应生成氯化银白色沉淀。要验证沉淀是否完全,可以取水层清液,继续滴加氯化钠溶液,若不出现白色沉淀,证明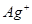 已经沉淀完全,反之则没有沉淀完全。
已经沉淀完全,反之则没有沉淀完全。
(2)沉淀转化的实质是向生成更难溶的方向进行,所以如果加入碘化钾,则白色沉淀转化为黄色沉淀碘化银。如果继续加入硫化钠,则黄色沉淀转化为黑色硫化银。
(3)根据反应物的生成物可写出该反应的方程式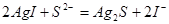 。
。
本题难度:一般
5、选择题 在无色透明的碱性溶液中下列各组离子能大量共存的是( )
A.K+,Cu2+,Cl-,SO42-
B.Na+,Mg2+,NO3-,SO42-
C.Na+,SO42-,Ca2+,Cl-
D.K+,SO42-,CO32-,Cl-
参考答案:A.因Cu2+与OH-结合生成沉淀,且Cu2+在水中为蓝色,与无色溶液不符,故A错误;
B.因OH-与Mg2+结合生成沉淀,则不能共存,故B错误;
C.因SO42-、Ca2+能结合生成硫酸钙微溶物,则不能共存,故C错误;
D.碱性溶液中该组离子之间不反应,则能够共存,且离子均为无色,故D正确;
故选D.
本题解析:
本题难度:简单