1、计算题 一块表面已部分被氧化的钠的质量为0.77 g,放入10 g水中后,得到氢气0.02 g。求:
(1)金属钠表面氧化钠的质量;
(2)所得溶液的质量分数;
(3)被氧化前这块钠的质量。
参考答案:(1)0.31 g
(2)11.2%
(3)0.69 g
本题解析:该样品成分为Na、Na2O,由得到H2的量可以求出Na的量,再由样品总量可求出Na2O的量。
(1)2Na+2H2O====2NaOH+H2↑
46? 80? 2
x? y? 0.02 g
解得x="0.46" g y="0.8" g
m(Na2O)="0.77" g-0.46 g="0.31" g
(2)Na2O+H2O====2NaOH
62? 80
0.31 g? z
解得z="0.4" g
(NaOH)=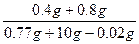 ×100%=11.2%
×100%=11.2%
(3)2Na―Na2O
46? 62
p? 0.31 g
解得p="0.23" g
m(Na)总="0.23" g+0.46 g="0.69" g。
本题难度:简单
2、选择题 在泡沫灭火器中放NaHCO3而不用Na2CO3,下列解释不合理的是
A.与酸反应时,NaHCO3放出CO2的速度更快
B.NaHCO3受热较易分解
C.等质量NaHCO3与Na2CO3,前者产生CO2气体多
D.NaHCO3比Na2CO3昂贵
参考答案:B
本题解析:本题考查应用化学知识解释实际化学问题的能力。泡沫灭火器中所以用NaHCO3而不用Na2CO3,应从灭火效力上考虑,即NaHCO3灭火效力大。在同样条件 下,NaHCO3与H+反应产生CO2的速度比NaCO3的速度快,更有利于快速灭火。1mLNaHCO3和Na2CO3都产生1mol CO2,但前者为84g,后者为106g,所以在盛重一定的灭火器内,装NaHCO3比装Na2CO3产生的CO2多,也有利于灭火。所以A,C的解释是正确的。显然B不是合理的解释。
本题难度:一般
3、选择题 下列关于碳酸氢钠的叙述,不正确的是(?)
A.它是一种白色粉末,易溶于水
B.其分子式为NaHCO3・10H2O,在空气里易风化
C.可以跟氢氧化钠起反应,生成正盐
D.与碳酸钠相比,若质量相同,分别跟足量的盐酸反应,碳酸氢钠得到的CO2多
参考答案:B
本题解析:碳酸氢钠是一种酸式盐。在钠盐中,不管是酸式盐还是正盐均易溶于水,故NaHCO3与食盐相似,是白色粉末,可溶于水,A项正确。NaHCO3的分子中不含结晶水,在空气里也没有易风化的性质,B项不正确。NaHCO3可以和NaOH反应,NaHCO3+NaOH====Na2CO3 +H2O,C项正确。D项正确,因此设各取106 g,则
Na2CO3+2HCl====2NaCl+H2O+CO2↑
106? 44
106 g? x
x="44" g
NaHCO3+HCl====NaCl+H2O+CO2↑
84? 44
106 g? y
y="55.5" g
本题难度:一般
4、选择题 钡和钠相似,也能形成含 的过氧化物,下列叙述中不正确的是(? )
的过氧化物,下列叙述中不正确的是(? )
A.过氧化钡的化学式是BaO2
B. 的电子式是[
的电子式是[ ]2-
]2-
C.1 mol Na2O2或BaO2跟足量的水反应都生成0.5 mol O2
D.过氧化钠和过氧化钡都是强氧化剂
参考答案:B
本题解析:BaO2可由Na2O2来类推,2BaO2+2H2O2Ba(OH)2+O2↑, 的电子式为[
的电子式为[ ]2-,故选B。
]2-,故选B。
本题难度:简单
5、选择题 200℃时,11.6 g CO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6 g,再将反应后剩余固体密封冷却后加入含有Na+、HCO、SO、CO等离子的水溶液中,假设加入后溶液体积保持不变,则下列说法中正确的是
A.原混合气体中CO2和水蒸气各0.25mol
B.混合气体与Na2O2反应过程中电子转移的物质的量为0.50 mol
C.溶液中SO的物质的量浓度基本保持不变
D.溶液中HCO的物质的量浓度减小,CO的物质的量浓度增大,但是HCO和CO的物质的量浓度之和基本保持不变
参考答案:B
本题解析:略
本题难度:一般