|
高考化学知识点总结《氯及其化合物》在线测试(2017年最新版)(十)
2018-03-17 05:40:02
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色.甲瓶中所盛的试剂可能是( )
①浓H2SO4?②NaOH溶液?③饱和NaCl溶液.
A.①③
B.③
C.①②
D.②③
| 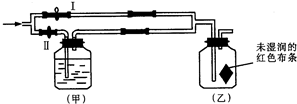
参考答案:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶,布条不褪色,若关闭Ⅱ阀打开Ⅰ阀,再通入这种气体,布条褪色,则
①氯气经过浓硫酸被干燥,干燥的氯气不能使有色布条褪色,故①正确;
②氯气通过NaOH溶液被吸收,气体经过甲瓶后,通入乙瓶,布条不褪色,故②正确;
③而通过饱和NaCl溶液后,细润的氯气可将红色布条漂白,故③错误.
故选C.
本题解析:
本题难度:简单
2、选择题 下列叙述中,不正确的是
[? ]
A.氯水中的次氯酸具有杀菌消毒作用 ?
B.陶瓷的主要成分是碳酸钙
C.硅是制造半导体的常用材料 ?
D.漂白粉的有效成分是次氯酸钙
参考答案:B
本题解析:
本题难度:简单
3、填空题 (6分) 氯元素有多种化合价,下列是按氯元素化合价由低到高排列的多种物质:NaCl、?、HClO、Ca(ClO)2、KClO3。请根据题意选择合适的化学式填空:
(1)根据氯元素的化合价变化,横线上应该填的物质为?;
(2)上述含氯化合物中,其固体能用于实验室制备氧气的是?;
(3)上述含氯化合物中,其水溶液有弱酸性和漂白性的是?。
参考答案:
(1)Cl2?(2)KClO3
(3)HClO
本题解析:略
本题难度:简单
4、填空题 为了探究三种气态氧化物(SO2、NO2、CO2)的性质,某同学设计了一组实验:
实验一:探究三种气体在水中的溶解性,用三支相同的试管收集满三种气体,倒置在盛满水的烧杯中,一段时间后,观察到的现象如图A、B、C所示。

(1)在相同条件下,三种气体在水中溶解度最大的是________(写化学式)写出A烧杯中发生反应的化学方程式:____?。如果在三只烧杯中分别滴几滴紫色石蕊试液,可观察到的现象是_____________________?。
实验二:用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量O2或Cl2,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。
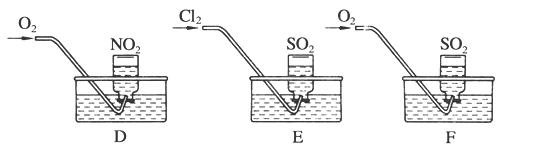
(2)实验二中装置D的集气瓶最终充满溶液(假设瓶内液体不扩散):
①写出装置D中总反应的化学方程式:
_______________________________________________。
②假设该实验条件下,气体摩尔体积为a L・mol-1。则装置D的集气瓶中所得溶液溶质的物质的量浓度为____________________。
(3) 写出实验F通入氧气后,发生反应的化学方程式:____________________________。
(4)溶液充满集气瓶后,在E装置的水槽里滴加硝酸钡溶液,可能观察到的现象为________,用有关的离子方程式解释原因:________________________。
参考答案:(1)NO2
3NO2+H2O=2HNO3+NO?溶液都变红色
(2)①4NO2+O2+2H2O=4HNO3?②1/a mol・L-1
(3) 2SO2+O2+2H2O=2H2SO4
(4)出现白色沉淀? Cl2+SO2+2H2O=2Cl-+SO+4H+? Ba2++SO=BaSO4↓
本题解析:(1)NO2在水中的溶解度最大;A试管剩余气体的体积为试管体积的1/3,所以A中气体为NO2,NO2与H2O反应的方程式为:3NO2+H2O=2HNO3+NO;SO2与H2O反应生成H2SO3,NO2与H2O反应生成HNO3,CO2与水反应生成H2CO3,都显酸性,滴入石蕊试液变红。
(2)①由3NO2+H2O=2HNO3+NO和2NO+O2=2NO2,可推出总反应化学方程式为:4NO2+O2+2H2O=4HNO3
②设集气瓶的体积为VL,则充满的NO2也为VL,HNO3的浓度为:VL÷aL/mol÷VL=1/a mol・L-1。
(3)O2氧化SO2,化学方程式为: 2SO2+O2+2H2O=2H2SO4
(4)Cl2在H2O存在的条件下把SO2氧化,生成SO42?,SO42?与Ba2+反应生成BaSO4沉淀,试液现象为:出现白色沉淀;反应的离子方程式为:Cl2+SO2+2H2O=2Cl-+SO+4H+ Ba2++SO=BaSO4↓。
本题难度:一般
5、计算题
(1)S(Na2CO3)与a的关系式,S=_____________(S代表溶解度)。
(2)a的取值范围。
参考答案:
(1) S=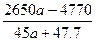 g? (2) a>1.8 g? (2) a>1.8
本题解析:(1)最后所得晶体质量为(a+1.06)g,其中含Na2CO3质量是:106(a+1.06)/286 g,含水质量为:180(a+1.06)/286 g;则:
S=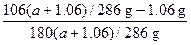 ×100 g= ×100 g=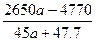 g g
(2)由于S>0,所以:2650a-4770>0,a>1.8。
本题难度:一般
| 