1、选择题 由菱镁矿(主要成分为MgCO3)制阻燃型氢氧化镁的工艺流程如下:
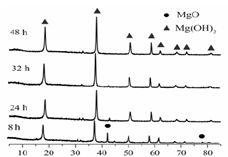
(1)从下面两图可以得出的结论为?、?。
 ?
?
图1 25℃时MgO水化随时间变化X射线衍射谱图?
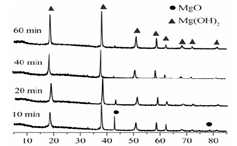
图2 90℃时MgO水化随时间变化X射线衍射谱图
(2)水化反应MgO+H2O = Mg(OH)2能自发进行的原因是?。
(3)结合元素周期律和表1可知,金属氢氧化物受热分解的规律有?。(写一条即可)
表1 ?部分主族元素的金属氢氧化物热分解温度/℃
LiOH
| NaOH
| KOH
| Al(OH)3
| Mg(OH)2
| Ca(OH)2
| Ba(OH)2
|
924
| 不分解
| 不分解
| 140
| 258
| 390
| 700
|
?
(4)已知热化学方程式:Mg(OH)2 (s) =" MgO" (s)+H2O (g)? ΔH =" 81.5" kJ・mol-1
①Mg(OH)2起阻燃作用的主要原因是?。
②与常用卤系(如四溴乙烷)和有机磷系(磷酸三苯酯)阻燃剂相比,Mg(OH)2阻燃剂的优点是?。
参考答案:(1)随着水化时间延长,MgO的量不断减少,Mg(OH)2的量不断增加 ;温度升高,水化反应速率加快。
(2)ΔH < 0
(3)金属离子半径越大,氢氧化物越难分解(或金属性越强,氢氧化物越难分解等)
(4)①Mg(OH)2分解时吸热,使环境温度下降;同时生成的耐高温、稳定性好的MgO覆盖在可燃物表面,阻燃效果更佳。②无烟、无毒、腐蚀性小
本题解析:该题工业流程作为背景设计了对图、表的解读能力及对化学反应条件、方向等方面知识的考查。(1)图1表达的是随时间的变化,MgO和Mg(OH)2的量的变化,图2给出的温度不同于图1,时间也不同于图5,由此得出结论。(2)反应的ΔS< 0,则反应ΔH < 0才有可能自发进行。(4)从燃烧的条件解释,反应吸热而使温度降低,生成耐热材料覆盖可燃物表面阻止燃烧进一步进行。有机和卤系阻燃剂会产生烟、有机磷系有毒,也会生成有毒物质。
本题难度:一般
2、填空题 以地下卤水(主要含NaCl,还有少量Ca2+、Mg2+)为主要原料生产亚硫酸钠的新工艺如下,同时能得到用作化肥的副产品氯化铵。

已知以下四种物质的溶解度曲线图:
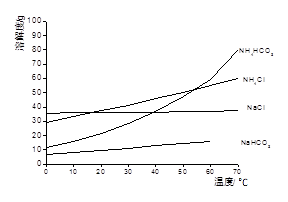
(1)“除杂”时,先加入适量石灰乳过滤除去Mg2+,再通入CO2并用少量氨水调节pH过滤除去Ca2+,“废渣”的主要成分为 ?、?。
(2)“滤渣1”的化学式为?。
(3)在“滤液1”中加入盐酸的目的是?。“滤渣2”的化学式为?。
(4)已知H2CO3和H2SO3的电离常数如下表,“通入SO2”反应的化学方程式为?。
物质
| 电离常数(25℃)
|
H2CO3
| K1=4.4X10-7?K2=4.7X10-11
|
H2SO3
| K1=1.23X10-2?K2=5.6X10-8
|
?
参考答案:(16分)(1)Mg (OH)2(2分)? CaCO3(2分)
(2)NaHCO3(3分)
(3)除去HCO3-(3分,多答“使更多的Na+形成NaCl析出,提高NH4Cl的纯度”不扣分)?NaCl(3分)
(4)NaHCO3+SO2 = NaHSO3+ CO2(3分)
本题解析:(1)依题意,除杂步骤涉及的反应为Ca(OH)2+Mg2+=Mg(OH)2+Ca2+,CO2+2NH3?H2O=2NH4++CO32-+H2O,Ca2++CO32-=CaCO3↓,则废渣的主要成分是Mg(OH)2、CaCO3;(2)由溶解度曲线可知,NaHCO3的溶解度最小,最先达到饱和,则NH4HCO3与饱和NaCl具备发生复分解反应发生的条件,即NH4HCO3+NaCl=NaHCO3↓+NH4Cl,因此滤渣1的主要成分是NaHCO3;(3)过滤后滤液1中的主要成分是NaCl、NH4Cl、NaHCO3,氯化纳和氯化铵都不能与盐酸反应,而碳酸氢钠与盐酸能反应,即HCO3-+H+=CO2↑+H2O,因此加入足量盐酸能除去HCO3-,提高NH4Cl的纯度;由溶解度曲线可知,热溶液中NaCl的溶解度小于NH4Cl,因此蒸发浓缩、趁热过滤得到的滤渣2为NaCl,而滤液则含有NH4Cl、NaCl;由于NH4Cl的溶解度随温度降低明显减小,而NaCl的溶解度随温度降低无明显变化,则蒸发浓缩、冷却结晶可制备NH4Cl晶体;(4)滤渣1为NaHCO3,根据表中的电离常数可知电离程度:H2SO3>H2CO3>HSO3->HCO3-,根据复分解反应发生的条件可知,通入SO2的反应为NaHCO3+SO2=NaHSO3+CO2,不可能为2NaHCO3+SO2=Na2SO3+2CO2+H2O,因为CO2+H2O+Na2SO3= NaHSO3+NaHCO3。
本题难度:困难
3、填空题 (8分)2004年10月1日,南昌八一广场以全新的面貌重新向市民开放,成为南昌的一大亮点。在这次改造扩建的过程中采用了大量的花岗石(不与常见酸反应)和大理石。要区别这两种石料,正确的操作是________________________________________________。
参考答案:分别向两种石料样品上滴加稀盐酸或稀硝酸,有气泡产生的为大理石,无气泡产生的则为花岗石。?
本题解析:大理石、石灰石的主要成分都为碳酸钙,可通过加稀盐酸或硝酸反应产生气泡鉴别,花岗石的主要成分是一些硅酸盐,不与常见酸反应,所以加酸后不会产生现象。
本题难度:简单
4、填空题 自洁面料就是在普通的面料纤维中加入一层薄薄的纳米二氧化钛。含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取纳米级TiO2的流程如下:
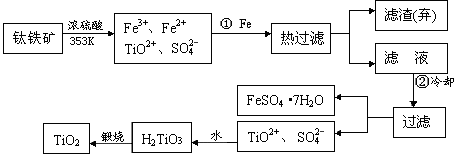
(1)Ti的原子序数为22,Ti位于元素周期表中的第________周期,第______族。
(2)步骤①加铁的目的是_________________;步骤②冷却的目的是_______________。
(3)上述制备二氧化钛的过程中,可以利用的副产物是______________;考虑成本和废物综合利用因素,废液中应加入___________________处理。
(4)由金红石制备单质钛,涉及到的步骤为:
TiO2 TiCl4
TiCl4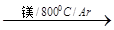 Ti?
Ti?
已知:①C(s)+O2(g)==CO2(g)?△H= -393.5kJ・mol-1
②2CO(g)+O2(g)==2CO2(g)?△H= -5665kJ・mol-1
③TiO2(s)+2Cl2(g)==TiCl4(s)+O2(g)?△H= +41kJ・mol-1
则TiO2(s)+ 2Cl2(g)+C(s)==TiCl4(s)+2CO(g)的△H=____________。
反应TiCl4+2Mg == 2MgCl2+Ti 在氩气氛中进行的理由是________________________。
参考答案:(1)4;IVB
(2)将Fe3+还原为Fe2+;析出(或分离、或得到)FeSO4・7H2O
(3)FeSO4・7H2O;石灰(或碳酸钙、废碱)
(4)-80kJ・mol-1;防止高温下镁和钛与空气中氧气(或二氧化碳、或氮气)作用
本题解析:用框图形式给出工业生产流程,让考生面对自己观察框图,获取所需信息解决问题,这类试题体现了新课程改革的方向。试题有一定难度,考查吸收信息、处理信息等综合分析能力。
(1)可以根据钙元素的位置推断钛元素的位置,该元素位于周期表第四周期IIA主族,故钛位于IVB;
(2)观察题给流程图可知,所得产品有FeSO4・7H2O和TiO2两种。由于加浓硫酸后所得溶液含有Fe3+,所以步骤①中加入铁是为了将Fe3+转化成Fe2+。步骤②冷却是为了降低硫酸亚铁的溶解度,使硫酸亚铁结晶析出;
(3)该流程的主要目的是制取二氧化钛,故其是主要产品,则FeSO4・7H2O是副产品。废液处理时,根据流程分析废液可能会剩余部分酸,故可以考虑加入石灰或其它废碱,以将酸中和掉;
(4)运用盖期定律可计算出反应热。由于高温条件下金属镁易跟氧气、二氧化碳等气体发生反应,所以应充入氩气来保护镁。
本题难度:一般
5、选择题 将过量的CO2分别通入①CaCl2溶液,②Na2SiO3溶液,③Ca(ClO)2溶液,④饱和Na2CO3溶液,最终有沉淀析出的是( )
A.①②③④
B.②④
C.①②③
D.②③
参考答案:B
本题解析:
本题难度:简单