1、填空题 在实验室中做如下实验:一定条件下,在容积为2.0L的恒容密闭容器中,发生如下反应:?
2A(g)+B(g)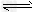 2C(g);△H?=QkJ/mol
2C(g);△H?=QkJ/mol
(1)若A、B起始物质的量均为零,通入C的物质的量(mol)随反应时间(min)的变化情况如下表
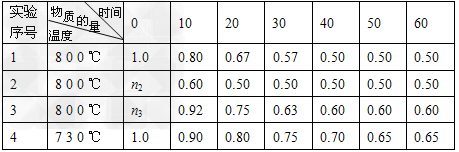
根据上表数据,完成下列填空:
①在实验1中反应在10至20min内反应的平均速率Vc=______mol/(L・min);实验2中采取的措施是________;实验3中n3_____1.0?mol(填“>、=、<”)。
②比较实验4和实验1,可推测该反应中Q________0(填“>、=、<”),理由是____________________________
(2)在另一反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断下列说法正确的_____________
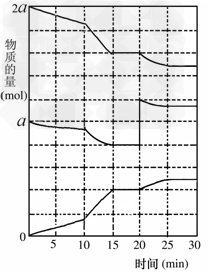
a.10~15?min可能是升高了温度?
b.10~15?min可能是加入了催化剂
c.20?min时可能是缩小了容器体积?
d.20?min时可能是增加了B的量
(3)一定条件下,向上述容器中通入5molA?(g)和3molB(g),此时容器的压强为P(始)。反应进行并达到平衡后,测得容器内气体压强为P(始)的7/8?。若相同条件下,向上述容器中分别通入a?molA(g)、b?molB(g)、c?molC(g),欲使达到新平衡时容器内气体压强仍为P(始)的7/8?。 ①a、b、c必须满足的关系是_______、________(一个用a、c表示,另一个用b、c表示)
②欲使起始时反应表现为向正反应方向进行,则a的取值范围是______________。
参考答案:(1)①?v(c)?=0.0065mol/(L・min?)?;使用催化剂;?>;②<;温度越低,C的平衡浓度升高,说明正反应放热
(2)abd
(3)①a-c=5;b?─c/2=3;?②3?<a?≤5。
本题解析:
本题难度:一般
2、选择题 在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)
2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
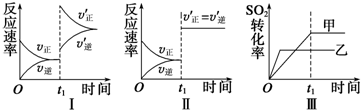
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
参考答案:A.增大氧气的浓度,瞬间逆反应速率不变,图中不符,应为增大压强,故A错误;
B.图Ⅱ正正逆反应速率同等程度的增大,为催化剂对反应的影响,故B正确;
C.催化剂不改变平衡,应为压强对反应的影响,故C错误;
D.乙先达到平衡,压强大,且压强大,转化率增大,转化率与图象不符合,故D错误;
故选B.
本题解析:
本题难度:一般
3、选择题 某密闭容器中发生如下反应:X(g)+3Y(g)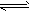 2Z(g) △H<0
2Z(g) △H<0

上图表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的用量。下列说法中不正确的是
[? ]
A.t2时加入了催化剂
B.t3时减小了压强
C.t5时升高了温度
D.t4~t5时间内反应物的转化率最低
参考答案:D
本题解析:
本题难度:一般
4、选择题 某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g)?cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确的是( )
A.平衡正向移动
B.平衡逆向移动
C.Z的体积分数变大
D.(a+b)>(c+d)
参考答案:持温度不变压强增大至原来的2倍,将容器的容积压缩到原来容积的一半,假定平衡不移动,W浓度变为原来的2倍,达到新平衡时,物质W的浓度是原来的1.8倍,说明平衡向逆反应方向移动,则应由a+b<c+d,
A.由上述分析可知,增大压强平衡向逆反应移动,故A错误;
B.由上述分析可知,增大压强平衡向逆反应移动,故B错误;
C.平衡向逆反应移动,Z的体积分数减小,故C错误;
D.平衡向逆反应方向移动,则应由a+b<c+d,故D错误;
故选B.
本题解析:
本题难度:简单
5、填空题 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。

(1)体系中发生反应的化学方程式是___________________________
(2)列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________
(3)该反应达到平衡时反应物X的转化率等于___________________________
(4)如果该反应是放热反应。改变实验条件(温度.压强.催化剂)得到Z随时间变化的曲线①.②.③(如图所示)则曲线①.②.③所改变的实验条件和判断理由是

① __________________________
② __________________________
③ __________________________
参考答案:(1)X+2Y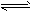 2Z
2Z
(2)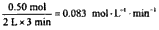
(3)45%
(4)①升高温度,该反应为放热反应 达到平衡的时间缩短,平衡时Z的浓度减小
②加入催化剂,达到平衡的时间缩短,平衡时Z的浓度减小
③增大压强,达到平衡的时间缩短,平衡时Z的浓度增大
本题解析:
本题难度:困难