1��ѡ���� ��ij��ɫ������Һ�У��ܴ���������������ǣ�������
A��Na+��NH
��OH-��HCO
B��Cu2+��K+��SO��NO
C��Na+��K+��Cl-��NO
D��Fe3+��H+��SO��CH3COO-
�ο��𰸣�A����NH4+��OH-�������������ʣ�OH-��HCO3-�������ˮ�����ܹ��棬��B����
B����������֮�䲻��Ӧ���ܹ��棬��Cu2+Ϊ��ɫ������ɫ��Һ��������B����
C����������֮�䲻��Ӧ���ܹ��棬�����Ӿ�Ϊ��ɫ����C��ȷ��
D��H+��CH3COO-�������������ʴ��ᣬ���ܹ��棬��D����
��ѡC��
���������
�����Ѷȣ�һ��
2��ѡ���� ���и��������У�������Һ�д���������ǣ�������
A��Ba2+��Cl-��Na+��SO42-
B��Na+��OH-��K+��NO3-
C��Ca2+��NO3-��K+��CO32-
D��Fe3+��Cl-��Ag+��OH-
�ο��𰸣�A����Ba2+��SO42-������ɳ��������ܹ��棬��A����
B�����������֮�䲻��Ӧ�����ܹ����棬��B��ȷ��
C����Ca2+��CO32-������ɳ��������ܹ��棬��C����
D����Fe3+��OH-������ɳ�����Cl-��Ag+������ɳ��������ܹ��棬��D����
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� �±�������ͬ�¶����������һЩ���ݣ������ж���ȷ���ǣ�?��
��
| HX
| HY
| HZ
|
Ũ�ȣ�mol/L��
| 0.12
| 0.2
| 0.9
| 1
| 1
|
�����
| 0.25
| 0.2
| 0.1
| 0.3
| 0.5
|
���볣��
| K1
| K2
| K3
| K4
| K5
|
?
A������ͬ�¶ȣ���HX�����ݿ���˵�������������Һ��Ũ��Խ�ͣ������Խ����K1��K2��K3=0.01
B������ʱ������NaZ��Һ�м�ˮ����c��Z-��/ [c��HZ��? c��OH-��]�ı�ֵ��С�������������ᣬ���ֵ���
C�������ʵ�����NaX��NaY��NaZ�Ļ�ϣ�c��X-��+c��Y-��-2c��Z-��=2c��HZ��-c��HX��-c��HY������c��Z-��<c��Y-��<c��X-��
D������ͬ�¶��£�K5��K4��K3
�ο��𰸣�D
���������A��K1��K2��K3=0.009������B��NaZ��ǿ�������Σ�Z����H2O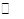 ?HZ��OH����������ʱ��ˮ�ⳣ���Ƕ�ֵ����c��Z-��/ [c��HZ��? c��OH-��]�ı�ֵ����ˮ�ⳣ���ĵ����������ֵ����Ũ�ȵı仯���仯������C����ΪHZ�ĵ���̶ȱ�HY������У� c��Z������c��Y����������D��ͨ�������֪����ȷ��
?HZ��OH����������ʱ��ˮ�ⳣ���Ƕ�ֵ����c��Z-��/ [c��HZ��? c��OH-��]�ı�ֵ����ˮ�ⳣ���ĵ����������ֵ����Ũ�ȵı仯���仯������C����ΪHZ�ĵ���̶ȱ�HY������У� c��Z������c��Y����������D��ͨ�������֪����ȷ��
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
A���ڴ�ˮ�м�������ٽ�ˮ�ĵ���
B��1 mL pH = 2�Ĵ���ϡ����10 mL��pH=3
C�������£�0.1 mol��L �C1�Ȼ����Һ��ˮϡ�ͣ���Һ����������Ũ�Ⱦ���С
D������Na2CO3��Һ�����������۵�����
�ο��𰸣�D
����������������ᣬ�ܵ���������ӣ�����ˮ�ĵ��룬A����ȷ��������Һ�д��ڵ���ƽ�⣬ϡ�ʹٽ����룬�����ӵ����ʵ��������ӵģ����1 mL pH = 2�Ĵ���ϡ����10 mL��pH��3��B����ȷ��ϡ���Ȼ�林ٽ�ˮ�⣬�����ӵĸ������ӣ���������Ũ���Ǽ�С�����OH-��Ũ�������ӵģ�C����ȷ�����ȴٽ�̼���Ƶ�ˮ�⣬��Һ�ļ�����ǿ�����Կ���������۵�������D��ȷ����ѡD��
���������ж���Һ������Ũ�ȴ�Сʱ�����뿼�ǵ���Һ����ı仯�������ܽ�������ƽ����ƶ�������β����ǵ���ƽ�⣬����ˮ��ƽ�ⶼ��������������ԭ�����ݴ˿��Խ����й��жϡ�
�����Ѷȣ�һ��
5��ѡ���� ��1mol��L-1H2SO4��Һ100mL����������Ϊ10%��NaOH��Һ50g��Ͼ��Ⱥ������ָʾ������ʱ��Һ����ɫ��
A��dz��ɫ
B����ɫ��
C����ɫ��
D����ɫ
�ο��𰸣�C
��������������ṩ��H+Ϊ0.2 mol��NaOH�ṩ��OH��Ϊ0.125 mol��������Һ��c(H+)=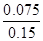 =0.5mol/L��pH=0.3�����ݼ��ȵı�ɫ��Χ��֪��������Һ����ɫΪ��ɫ
=0.5mol/L��pH=0.3�����ݼ��ȵı�ɫ��Χ��֪��������Һ����ɫΪ��ɫ
�����Ѷȣ�һ��