1、选择题 下列说法正确的是
[? ]
A.Al2O3难溶于水,不跟水反应,所以它不是Al(OH)3对应的氧化物
B.因为Al2O3是金属氧化物,所以它是碱性氧化物
C.Al2O3能跟所有的酸碱溶液反应
D.Al2O3能跟强的酸碱溶液反应
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的物质是 (?)
①NaHCO3?②Al2O3?③Al(OH)3?④Al? ⑤(NH4)2CO3
A.全部
B.①②③
C.①②③⑤
D.②③④
参考答案:A
本题解析:根据所给物质的化学性质可知,选项中所有物质都能和稀硫酸以及氢氧化钠溶液反应,答案选A。
点评:该题是基础性试题的考查,难度不大。该题的关键是记住常见既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的物质,学生不难得分。
本题难度:一般
3、选择题 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量关系可表示为
[? ]
A. 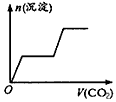
B. 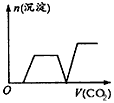
C. 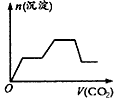
D. 
参考答案:C
本题解析:
本题难度:一般
4、填空题 某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝,流程如下,回答下列问题:
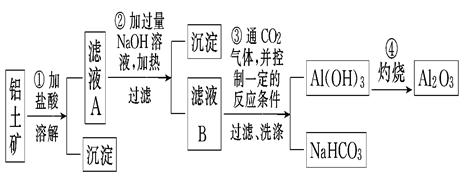
(1)画出Al的原子结构示意图?。
(2)写出反应①中主要成分发生反应的化学方程式:?。
(3)写出滤液B中溶质的化学式?。
(4)甲同学在实验室中用如左下图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。乙同学分析认为:甲同学通入的CO2中含有HCl气体,是导致实验失败的原因。乙同学认为在实验装置Ⅰ和装置Ⅱ之间增加右下图装置可解决这个问题。请在右下图装置的横线上注明试剂名称。
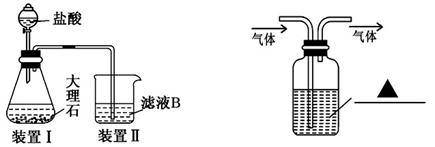
(5)工业上通常以铝土矿提取得到的Al2O3为原料制备无水氯化铝:
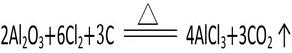
该反应中的还原剂是?,若制得22.4 L(标准状况下)CO2气体时,则有?mol电子发生转移。
参考答案:(12分)(1) 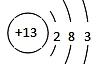 ?[2分]
?[2分]
(2)Al2O3+6HCl=2AlCl3+3H2O [2分,若多写Fe2O3与HCl反应不扣分]
(3)NaAlO2、NaCl、NaOH [2分,只要写出NaAlO2、NaCl即给分,答对一个给1分]
(4)饱和碳酸氢钠溶液?[2分,写成化学式也给分,“饱和”未写不扣分]
(5)C(或碳),? 4?[每空2分]
本题解析:(1)Al的原子序数是13,所以Al的原子结构示意图是 。
。
(2)盐酸和氧化铝、氧化铁反应,但和二氧化硅不反应。由于主要成分是氧化铝,所以反应的方程式是Al2O3+6HCl=2AlCl3+3H2O。
(3)由于氢氧化铝是两性氢氧化物,所以A中加入过量的氢氧化钠溶液时生成偏铝酸钠,则B中溶质的主要成分是NaAlO2、NaCl、NaOH。
(4)要除去CO2中的氯化氢气体,应该利用饱和碳酸氢钠溶液。
(5)根据反应的方程式可知,碳元素的化合价从0价升高到+4价,失去4个电子,所以还原剂是碳。CO2的物质的量是22.4L÷22.4L/mol=1.0mol,则转移电子的物质的量是4mol。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,贴近高考,在注重对学生基础知识的巩固和训练的同时,侧重对学生基础知识的巩固和训练。有利于调动学生的逻辑推理能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该类试题主要是考查学生能够敏捷、准确地获取试题所给的相关信息,并与已有知识整合,在分析评价的基础上应用新信息的能力。
本题难度:一般
5、选择题 下列物质性质与应用对应关系正确的是
A.晶体硅熔点高硬度大,可用于制作半导体材料
B.氢氧化铝具有弱碱性,可用于制胃酸中和剂
C.漂白粉在空气中不稳定,可用于漂白纸张
D.氧化铁能与酸反应,可用于制作红色涂料
参考答案:B
本题解析:A、晶体硅能导电,可用于制作半导体材料,与熔点高硬度大无关系,A不正确;B、氢氧化铝具有弱碱性,能与酸反应生成铝盐和水,可用于制胃酸中和剂,B正确;C、漂白粉具有强氧化性,可用于漂白纸张,与其稳定性无关系,C不正确;D、氧化铁是红棕色粉末,可用于制作红色涂料,与是否能与酸反应无关系,D不正确,答案选B。
本题难度:一般